关于麻醉药及违禁药在抑郁症快速起效领域应用情况的调查研究
在关于快速抗抑郁的药物研究进展这一篇博客中,我们对快速抗抑郁药物的发展进行了一定的调查研究,在本篇博客中,我们将对快速抗抑郁药物中的麻醉药及违禁药再进行深入探讨,以拓展我们在快速抗抑郁药物领域的视野。
本篇博客涉及的药物,均为用于医学研究,不做其他用途,并且均可在PubMed查到相关文献信息
摘要
一些麻醉药已经显示出对抗抑郁症有潜在的效果。氯胺酮是最为人所知的一种,它具有急性、短暂的抗抑郁和抗自杀效果[1]。此外,一氧化二氮也显示出了抗抑郁效果 [1]。异氟醚和丙泊酚也有可能具有抗抑郁效果,但需要进一步研究[1]。
根据最新的研究,一些违禁药物,如麦角酸二乙胺(LSD)、骄子眼碱(Psilocybin)和死藤水(Ayahuasca)显示出快速抗抑郁的潜力。
下面让我们对麻醉药物以及违禁药物在抑郁症快速起效领域应用情况进行详细说明解释。
麻醉药物
Arketamine
在之前的关于快速抗抑郁的药物研究进展一文中,我们对氯胺酮(Arketamine)进行了一定的调查研究,这次我们再深入了解一下详细内容。美国食品药品监督管理局(FDA)批准了一种氯胺酮的鼻喷剂用于治疗抗药性抑郁症,这次就氯胺酮鼻喷剂进行详细说明。
氯胺酮鼻喷剂是一种用于治疗抗药性抑郁症的新型药物,主要成分为氯胺酮的更有效形式——鼻喷剂盐酸酮。
氯胺酮鼻喷剂的作用机制是通过与大脑中的受体结合,产生一种名为谷氨酸的化学物质,这种化学物质在调节情绪方面起着关键作用。低谷氨酸水平可能导致抑郁症状。此外,氯胺酮还可以刺激产生脑源性神经营养因子,这种蛋白质在神经可塑性中起作用,氯胺酮可能有助于改变导致抑郁的负面思维模式[2]。
氯胺酮鼻喷剂的一个主要优势是其快速起效的特性。与传统的抗抑郁药物相比,传统的抗抑郁药物可能需要几周的时间才能改善症状,而氯胺酮可能在1小时内就能提供缓解[2]。临床试验结果显示,使用氯胺酮鼻喷剂的患者在抑郁症状改善方面比使用安慰剂的患者有更大的改善。然而,尽管氯胺酮鼻喷剂在临床试验中显示出了降低抑郁症状的效果,但在现实世界的治疗效果仍需要进一步探索 [3]。
在一项针对FDA批准的氯胺酮鼻喷剂的III期临床试验中,研究人员发现,使用氯胺酮鼻喷剂的患者比使用安慰剂的患者有显著更多的改善。此外,症状的改善在首次剂量后的24小时内就开始出现,这突显了该药物的快速作用机制[4]。
在一项对氯胺酮鼻喷剂的益风险评估中,研究人员发现,每100名接受氯胺酮加口服抗抑郁药物治疗的患者中,有5-21名患者会达到缓解,14-17名患者会有反应。在维持治疗中,使用氯胺酮的患者复发的情况会少19-32例。在这两种情况下,严重或严重的常见不良事件(主要是解离、眩晕和头晕)的差异很小。这些发现支持氯胺酮加抗抑郁药物作为抗药性抑郁症患者的诱导和维持治疗具有积极的益风险平衡[5]。
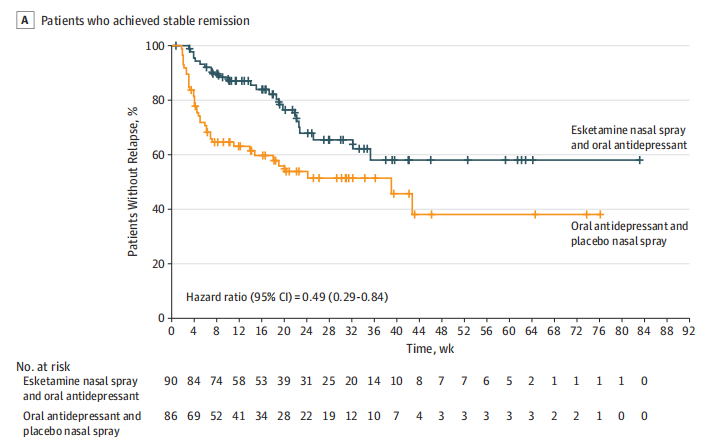
在一项随机临床试验中,研究人员发现,对于达到稳定缓解或稳定反应的抗药性抑郁症患者,继续使用氯胺酮鼻喷剂加口服抗抑郁药物治疗,比使用抗抑郁药物加安慰剂治疗,更能有效延迟抑郁症状的复发。氯胺酮和抗抑郁药物治疗降低了复发风险,对于达到稳定缓解的患者,降低了51%,对于达到稳定反应的患者,降低了70%[6]。
Esketamine
在之前的关于快速抗抑郁的药物研究进展一文中,我们对艾司氯胺酮(Esketamine)进行了一定的调查研究,这次我们再深入了解一下详细内容。
艾司氯胺酮(Esketamine)是氯胺酮的一种形式,被美国食品和药物管理局(FDA)在2019年批准用于治疗抗药性抑郁症。这种药物以鼻喷雾的形式出售,名为Spravato,用于治疗在尝试了两种或更多类型的抗抑郁药物后仍未见效的抑郁症症状。艾司氯胺酮比氯胺酮更有效,因此医生可以以较低的剂量进行处方,产生类似的效果。
Spavato
Spavato是一种含有活性药物麻黄碱酮的处方药,用于治疗抗药性抑郁症(至少尝试过两种其他抗抑郁药物后抑郁症仍未消退)和有自杀想法和行为的重度抑郁症[7]。
Spavato的作用机制是通过阻断N-methyl-D-aspartate (NMDA)受体,这种受体在大脑中产生一种名为谷氨酸的化学物质,而谷氨酸在调节情绪中起着关键作用[2][8]。
Spavato的一个主要优势是其快速起效的特性。传统的抗抑郁药物可能需要几周的时间才能改善症状,而Spavato可能在1小时内就能提供缓解[2]。
研究表明,Spavato在治疗抗药性抑郁症方面的效果可能在24小时内显现 [4]。然而,尽管Spavato具有这些优势,但它也可能引起一些副作用,包括恶心和呕吐、头晕、心跳加速、失眠、血压升高等[7]。
活性药物是指在体内经过生物转化后产生的药物代谢物,这些代谢物具有生物化学活性,并能产生治疗效果。活性药物代谢物可以分为活性、无活性和有毒三种类型。活性代谢物是具有治疗效果的生物化学活性化合物,无活性代谢物是既无治疗效果也无毒性的生物化学无活性化合物,有毒代谢物是具有各种有害效果的生物化学活性化合物,类似于活性代谢物。药物代谢主要发生在肝脏,但全身都可以找到代谢酶,这使得活性代谢物在全身循环中的浓度较低,这种现象被称为首过代谢[9]。
麻黄碱酮是从麻黄植物中提取的一种生物碱,也被称为麻黄碱。麻黄碱酮在中国已经被用作药物数千年,最初由Nagai在1885年分离和鉴定,然后在20世纪20年代初由Chen和Schmidt重新发现。麻黄碱酮对肾上腺受体的作用可以分为α和β两种效应,这是自主药理学历史上的一个决定性时刻。麻黄碱酮成为了非常流行和有效的哮喘治疗方法,特别是因为它可以口服,而当时的标准疗法肾上腺素则不能。然而,自1950年代末期以来,麻黄碱酮作为哮喘治疗的使用已经逐渐减少,现在在许多国家,麻黄和麻黄碱酮产品已经被禁止,因为它们是制造上瘾的甲基安非他明(冰毒)的主要来源[10]。
麻黄碱酮也被研究用于减肥和提高新陈代谢率。一些研究显示,麻黄碱酮可以增加静息代谢率——即你的身体在休息时燃烧的卡路里数量——这可能是由于你的肌肉燃烧的卡路里数量增加。麻黄碱酮还可以增强你的身体的脂肪燃烧过程。然而,由于安全问题,含有麻黄碱酮的补充剂在美国等多个国家被禁止 [11]。
Sevoflurane
七氟烷(Sevoflurane)是一种麻醉药,常用于手术室进行全身麻醉的诱导和维持。七氟烷的血溶性较低,无刺激性气味,可以快速且舒适地使用,其低溶解性有助于精确控制麻醉深度,以及快速平稳地诱导和恢复全身麻醉 [124][125]。七氟烷在美国有两种产品:Ultane(Abbott Laboratories, Inc.)和一种通用产品,七氟烷吸入麻醉剂(Baxter Healthcare Corp.)。这两种产品在疗效上被美国食品和药物管理局评为相等,但存在一些差异。Ultane是通过单步合成过程制成的,而通用七氟烷是通过三步过程制造的。Ultane包含>300 ppm的水,而通用七氟烷包含<或=130 ppm的水。Ultane采用塑料聚对苯二甲酸乙二酯聚合物瓶供应,而通用七氟烷采用漆线铝瓶供应[126]。
在一项临床病例研究中,一位抗药性抑郁症(TRD)患者接受了七氟烷治疗,结果显示七氟烷具有快速且持久的抗抑郁效果,副作用较少。此外,患者在神经认知测量方面也显示出显著的改善。然而,这些初步结果表明,需要进一步的临床试验来确定七氟烷在TRD患者中的独立疗效和安全性[127]。
七氟烷的作用机制相当复杂,涉及多个生物学过程。首先,七氟烷被认为可以增强抑制性突触通道活动并抑制兴奋性突触活动[128]。在大脑皮层神经元中,七氟烷可以显著增加GABA能抑制,同时减少谷氨酸NMDA活动[129]。此外,七氟烷还可以通过保护线粒体功能,降低血清中的丙氨酸和天冬氨酸转氨酶水平,从而保护肝脏免受缺血/再灌注损伤[130]。在心肌细胞中,七氟烷可以延长动作电位的持续时间,这是通过抑制大鼠心室肌细胞中的瞬时向外K电流来实现的[131]。在血管平滑肌中,七氟烷可以通过降低血管平滑肌中的i和抑制肌原纤维Ca2+敏感性来抑制去甲肾上腺素和氯化钾引起的收缩[132]。七氟烷的作用机制尚未完全明确,需要进一步的研究来阐明。
七氟烷优势可能在于其相对快速、强大且持久的抗抑郁效果,且缺乏电抽搐治疗(ECT)相关的不良认知效应[133]。传统抗抑郁药物通常需要几周时间才能发挥作用,而且可能需要尝试多种药物才能找到最有效的治疗方案[134][135]。这些关于七氟烷的研究仍处于初级阶段,需要进一步的研究来更好地理解这些药物的工作机制以及如何作为有效的抗抑郁疗法。
肌原纤维中的Ca2+(钙离子)在肌肉收缩和放松过程中起着关键作用。当肌肉细胞受到刺激时,钙离子从肌浆网(一种内质网的特殊形式)释放到细胞质中,与肌动蛋白和肌球蛋白相结合,触发肌肉收缩。收缩结束后,钙离子被重新吸收到肌浆网中,肌肉就会放松[136][137]。此外,钙离子还参与调节肌肉的能量代谢,例如通过激活糖原分解和糖酵解途径来提供ATP(肌肉收缩所需的能量源)[136]。
Scopolamine
东莨菪碱(Scopolamine)是一种非选择性毒蕈碱受体拮抗剂,已显示出相对快速的抗抑郁效果 [138][139]。
Scopolamine的作用机制可能超越了直接的毒蕈碱胆碱受体拮抗作用,其抗抑郁反应的时间和持久性暗示了Scopolamine诱导的基因表达和突触可塑性的变化可能提供了治疗机制[138]。
东莨菪碱是胆碱能受体的竞争性抑制剂。根据一项系统性回顾,东莨菪碱被发现可以作为一种有效且快速的抗抑郁药物,无论是单极性还是双极性抑郁症,其作用可能在首次输液后的3天内就开始发挥 [140]。另一项研究发现,东莨菪碱的抗抑郁效果是通过介导前额叶皮质中的GABA神经元实现的[141]。东莨菪碱也可能导致记忆损失,这可能与其对线粒体功能的影响有关[142]。
与传统的抗抑郁药物相比,Scopolamine的优势在于其快速和强大的抗抑郁效果。传统的抗抑郁药物通常需要几周的时间才能发挥全效,而Scopolamine的抗抑郁效果在首次输注后3天内就能显现,且临床改善持续时间超过2周[138][143]。需要注意的是,尽管Scopolamine显示出快速的抗抑郁效果,但其效果的持久性有限,且某些化合物的副作用需要管理[144]。
非选择性毒蕈碱受体拮抗剂是一种药物,它可以阻止毒蕈碱受体的活性,但不区分毒蕈碱受体的亚型。这些药物包括阿托品、托尔特罗丁和氧化丁丁等。阿托品是一种广泛使用的非选择性毒蕈碱受体拮抗剂,主要用于治疗器官磷酸酯中毒和由此引发的癫痫发作[145]。托尔特罗丁是一种非选择性毒蕈碱受体拮抗剂,用于治疗尿失禁,但在临床研究中,它与氧化丁丁一样有效,但引起的口干症状较少[146]。
胆碱能受体是神经系统中的一种受体,它们通过配体乙酰胆碱的激活而起作用。这些受体可以分为烟碱型和毒蕈碱型受体,这两种受体的命名源于它们的研究中使用的不同激活配体。烟碱型受体对尼古丁有反应,而毒蕈碱型受体对毒蕈碱有反应。这两种受体在功能上有所不同,分别作为离子型配体门控和G蛋白偶联受体。烟碱型受体在中枢神经系统和神经肌肉接头中起作用,而毒蕈碱型受体在周围和中枢神经系统中起作用,介导内脏器官的神经支配。这两种受体类型的信号转导差异赋予了受体激活时的不同生理功能。此外,受体亚型的差异为药物靶点和疾病发病机制创造了独特的影响[147]。
单极性抑郁症是一种常见的精神障碍,主要表现为持续的低落情绪、兴趣或愉快感丧失、疲劳感增强等症状。这种疾病可能会对患者的日常生活产生重大影响,包括工作、学习和社交活动。单极性抑郁症的诊断和治疗有着明确的指南,包括药物治疗、心理治疗以及互联网和移动设备基础的治疗等。此外,单极性抑郁症的治疗还强调了所有服务在护理抑郁症患者时的协调性[148]。
双极性抑郁症是一种严重的精神疾病,特征是情绪和能量状态的波动。这种疾病影响了全球超过1%的人口,不论国籍、种族起源或社会经济地位[149]。双极性抑郁症包括双极性I型和双极性II型。双极性I型病患者会经历至少一次躁狂发作,可能在躁狂发作前后经历轻躁狂发作或重大抑郁期。双极性II型病患者则会经历轻躁狂发作和重大抑郁期[150]。此外,双极性抑郁症的病患者常常伴有精神和医学的共病性[149]。治疗双极性抑郁症通常涉及药物治疗和心理社会干预策略[151]。
Nitrous oxide
一氧化二氮(Nitrous oxide),也被称为笑气,是一种无色无味的气体,已经在医学上使用了150多年,常被用作麻醉剂和镇痛剂。它是一种自由基,被发现是一个重要的信号分子,对心血管、神经和免疫系统有广泛的功能[12]。在神经系统中,一氧化氮被认为在调节多种神经递质系统,包括5-羟色胺、多巴胺、谷氨酸等,这些神经递质在抑郁症的发病机制中起着重要作用[13]。
一些临床和大量的预临床研究强烈建议一氧化氮信号通路在抑郁症和焦虑症中起作用,因此,一氧化氮系统可能是抗抑郁和抗焦虑药物在急性治疗和预防中的潜在靶点[14]。一项最近的双盲、前瞻性、交叉研究显示,一氧化二氮可以减轻一组严重病症的抗药性抑郁症患者的抑郁症状[15]。
一氧化氮的作用机制在于,它可以调节神经元钙离子通道中的钙离子流动,帮助调节神经元一氧化氮的产生。在一氧化氮缺乏的情况下,可能无法满足神经元对一氧化氮的需求,从而导致神经元损伤,这种损伤可能表现为抑郁症 [16]。
相比于传统的抗抑郁药物,一氧化氮的优势在于其可能更快地改善抑郁症症状。例如,一项研究报告了使用每餐和睡前服用125-300毫克的镁(作为甘氨酸和牛磺酸)治疗抑郁症,可以在7天内快速恢复 [16]。然而,这些研究结果仍需要进一步的临床试验来验证。
Lsoflurane
异氟醚(Isoflurane)是一种麻醉药,早期的研究表明它可能是电休克疗法(ECT)的有效替代品,对于那些对药物无反应但拒绝接受ECT的严重抑郁症患者可能有帮助。
一项研究发现,接受Isoflurane治疗的抑郁症患者在治疗后和4周随访时的抑郁程度都有显著降低,其抗抑郁效果接近ECT,但对认知的不良影响较小。然而,具体的作用机制尚不清楚,需要更大规模的临床试验来进一步研究[17]。
异氟醚的抗抑郁效果可能与其对神经递质的影响有关,但具体机制尚不清楚[18]。
与传统抗抑郁药相比,异氟醚的优势在于其快速起效和较少的认知副作用。研究发现,异氟醚治疗后,患者的抑郁症状有显著改善,且在治疗后和4周随访时,异氟醚患者的神经认知评分有更大的改善,而电击疗法患者在治疗后立即出现记忆、流畅性和处理速度的下降[19]。此外,异氟醚治疗的抑郁症患者在治疗期间的抗抑郁效果与电击疗法相当,且在随访期间进一步改善,而电击疗法患者则有复发的趋势[20]。
然而,需要注意的是,尽管异氟醚显示出抗抑郁效果,但目前的研究仍然有限,需要更大规模的临床试验来确认其效果和安全性[19]。
电休克疗法(Electroconvulsive Therapy,ECT)是一种非药物生物治疗,通过在全麻下向大脑传递电流以诱发全面性癫痫发作。这种治疗方法自1930年代以来已经发生了很大的变化,尽管它已经被优化以提高安全性并减少对认知的不良影响,但问题仍然存在。ECT已被证明是一种高效的治疗选择,主要用于治疗抑郁症,但也用于治疗精神分裂症和其他指标。尽管缺乏对长期治疗的受控研究,但ECT也可以用于维持疗法期间的复发预防。通过使用修改的刺激技术和现代麻醉的进步,电休克治疗的安全性和耐受性得到了提高。因此,今天也可以为具有较高体质风险的患者提供安全的治疗。尤其在药物治疗失败后的治疗抗药性精神疾病的疗法中,ECT仍然是一个重要的选择[21][22]。
Propofol
丙泊酚(Propofol)是一种常用于电击疗法(ECT)的麻醉药物。丙泊酚的使用在ECT文献中被频繁报道,尽管有人对其与其他麻醉药物相比可能导致更短的癫痫发作时间的倾向表示关注,但在手术麻醉文献中,丙泊酚显示出明显的优势,如改善的血流动力学和麻醉后恢复[23]。
丙泊酚的作用机制主要是通过激活GABA受体,增强γ-氨基丁酸(GABA)的抑制性神经传导,从而产生麻醉效果。
然而,丙泊酚对抑郁症的治疗效果并不明显。研究表明,丙泊酚与其他麻醉药物相比,确实与更短的癫痫发作时间有关,但抗抑郁效果似乎并未受到影响。丙泊酚的心率和血压变化不如其他药物高,麻醉后恢复可能更快[23]。
相比于传统的抗抑郁药物,丙泊酚的优势可能在于其对血流动力学的改善和麻醉后恢复的加快。然而,丙泊酚并不是主要的抗抑郁药物,因为其对抑郁症的治疗效果并不明显[23]。
氯胺酮异构体
S-氯胺酮
S-氯胺酮(Esketamine)是氯胺酮的对映异构体,是一种具有快速抗抑郁效果的药物,特别适用于治疗抗药性抑郁症。
S-氯胺酮通过阻断脑内谷氨酸N-甲基-D-天冬氨酸(NMDA)受体,产生抗抑郁效果。S-氯胺酮还可能通过其他机制发挥作用,包括选择性阻断含有NMDA受体亚基2B(NR2B)的NMDA受体亚型,抑制真核延长因子2(eEF2)激酶的磷酸化,增加脑源性神经营养因子(BDNF)和肌球蛋白受体激酶B(TrKB)的表达,以及激活哺乳动物雷帕霉素(mTOR)信号通路等[24]。
相比于传统的抗抑郁药物,S-氯胺酮的主要优势在于其快速起效。在给药后4.5小时内,超过60%的患者可以看到明显的抗抑郁效果,这种效果在24小时后仍然存在,7天后的反应率仍然超过40%。而传统的抗抑郁药物通常需要几周时间才能开始起效[24]。然而,S-氯胺酮的长期安全性仍有待进一步研究,包括潜在的神经认知和泌尿系统毒性,以及可能诱发物质使用障碍的风险 [24]。
真核延长因子2激酶(eEF2K)是一种非典型的’α-激酶’,它通过磷酸化并抑制真核延长因子2(eEF2)来减慢蛋白质合成的延长阶段,这个阶段通常消耗大量的能量和氨基酸。eEF2K的活性通常依赖于钙离子和钙调蛋白。最近的数据显示,eEF2K有助于保护癌细胞免受营养饥饿的影响,也在其他环境中具有细胞保护作用,包括缺氧。越来越多的证据表明,eEF2K在神经学过程中,如学习和记忆,甚至可能在抑郁症中也有作用[25]。
磷酸化是一种最常见且重要的蛋白质功能调控机制。这是一种急性且可逆的调控方式。研究表明,大约三分之一的所有细胞蛋白质通过蛋白质磷酸化进行共价修饰。磷酸化在细胞生物学的所有方面都起着重要的作用。大多数多肽生长因子(如血小板源性生长因子和表皮生长因子)和细胞因子(如白细胞介素2、集落刺激因子1和γ-干扰素)在与其受体结合后会刺激磷酸化。诱导的磷酸化反过来激活胞浆蛋白激酶,如Raf、丝裂原活化蛋白激酶(MAP)激酶SEK和MEK的激活剂、MAP激酶ERK、JNK和p38、Janus/JAK激酶、p21激活激酶(PAKs)以及磷脂酰肌醇3’-激酶激活的激酶、蛋白激酶B/Akt。此外,在所有有核生物中,细胞周期进程在G1/S和G2/M转换阶段都受到周期依赖性蛋白激酶的调控。这些激酶通过磷酸化细胞周期调控因子如Rb蛋白来调控G1/S转换,并通过磷酸化核纤维蛋白和组蛋白来调控G2/M转换[26][27]。
肌球蛋白受体激酶B(Akt)是一种丝氨酸/苏氨酸蛋白激酶,它在肌肉分化中起着重要的作用。Akt可以被磷脂酰肌醇3-激酶(PI 3-激酶)激活,从而显著增强肌管形成和肌肉特异性蛋白的表达,如MyoD,肌酸激酶,肌球蛋白重链和去斑蛋白。Akt的活性形式可以完全逆转PI 3-激酶抑制剂LY294002引起的肌肉分化抑制和肌肉特异性蛋白表达降低。这些结果表明,Akt可能是PI 3-激酶诱导肌肉分化的必要下游组分[28]。
哺乳动物雷帕霉素目标(mTOR)信号通路是一种关键的细胞信号通路,它在细胞生长、增殖、代谢和生存等多种生理过程中起着重要作用。mTOR是一种丝氨酸/苏氨酸蛋白激酶,它通过与特定的适配蛋白相互作用,形成两种不同的多蛋白复合体,即mTOR复合体1(mTORC1)和mTOR复合体2(mTORC2)[29][30]。mTORC1主要控制蛋白质合成、细胞生长、增殖、自噬、细胞代谢和应激反应,而mTORC2则主要调节细胞生存和极性[30][31]。mTOR信号通路的异常激活与多种疾病的发生和发展有关,包括癌症、心血管疾病、神经退行性疾病和各种肾脏疾病[30][31][32]。
R-氯胺酮
R-氯胺酮是氯胺酮的一种对映体,氯胺酮是一种麻醉药,也被用于抑郁症的治疗。
R-氯胺酮在抑郁症治疗中的作用机制可能与其对脑内谷氨酸N-甲基-D-天冬氨酸(NMDA)受体的阻断作用有关,这可能有助于改变负面的思维模式,从而改善抑郁症症状[2][24][33]。R-氯胺酮还能通过激活脑源性神经营养因子(BDNF)和cAMP反应元件结合蛋白(CREB)的信号通路,增加BDNF的表达,从而支持神经可塑性,这也可能有助于其抗抑郁效果[34]。
相比于传统的抗抑郁药,R-氯胺酮的一个主要优势是其快速起效的特性。传统的抗抑郁药可能需要几周的时间才能显现出改善症状的效果,而R-氯胺酮可能在1小时内就能提供缓解[2]。
R-氯胺酮的抗抑郁效果持久,且副作用较少[33][35]。然而,关于R-氯胺酮的长期效果和安全性,科学家们仍在进行研究[33]。
cAMP反应元件结合蛋白(CREB)是一种细胞内蛋白质,它调节对多巴胺神经元重要的基因的表达。多巴胺通过G蛋白偶联受体影响CREB的磷酸化。神经营养因子,如脑源性生长因子(BDNF),是神经发育和突触可塑性的关键调节器。CREB是神经营养因子反应的主要调节器之一,因为磷酸化的CREB绑定到BDNF启动子中的特定序列并调节其转录。此外,与精神分裂症相关的易感基因也针对并刺激CREB的活动。在精神分裂症患者的大脑中观察到CREB表达的异常,只在精神分裂症患者中发现了两种变体(-933T到C和-413G到A)。CREB也参与了动物模型的精神分裂症治疗。总的来说,这些发现表明CREB与精神分裂症的病理生理学之间存在联系[36]。
氯胺酮代谢物
(2R,6R)-HNK
关于(2R,6R)-HNK,在关于快速抗抑郁的药物研究进展中的化学遗传学策略提到过一嘴,接下来就来进行详细说明。
(2R,6R)-6-羟基诺氯胺(HNK)是一种抗抑郁药物,其作用机制与突然的压力敏感性、压力抗性、神经递质和代谢途径密切相关[37]。
HNK, I5和I6抗抑郁药物的研究发现,与对照组相比,HNK, I5和I6处理组中差异表达蛋白的数量分别为158,88和105。这些差异表达的蛋白主要具有结合、生物催化和运输的功能,主要参与细胞过程、生物调节过程、生物代谢过程和应激反应过程。GO和KEGG通路分析发现,这些差异表达的蛋白涉及长期增强、G13通路、血小板激活通路和MAPK信号通路 [37]。
相比于传统的抗抑郁药物,HNK的优势在于其快速起效。一项研究发现,与安慰剂相比,鼻内使用HNK可以显著且迅速地改善抑郁症状[38]。这对于那些传统抗抑郁药物无效的抑郁症患者来说,是一个重要的治疗选择。
HNK可以指两种不同的物质。一种是人类天然杀伤细胞-1抗原(Human Natural Killer-1,HNK-1),这是一种糖类抗原,参与多种神经事件,如神经纤维生成、髓鞘形成、突触可塑性以及神经系统受伤后的再生[39]。另一种是钩吻素(Honokiol,HNK),这是一种从传统中药木兰树皮中提取的活性化合物,已显示出强大的抗癌活动[40]。
GO通路(Gene Ontology pathway)是一种生物信息学工具,用于描述基因和基因产品在细胞中的角色。GO通路包括三个主要方面:生物过程(Biological Process),细胞组分(Cellular Component)和分子功能(Molecular Function)。生物过程描述了基因产品参与的过程,如代谢过程或信号传导;细胞组分描述了基因产品在细胞中的位置,如细胞核或质膜;分子功能描述了基因产品在分子层面上的活动,如酶活性或结合活性。GO通路可以帮助研究人员理解基因和基因产品如何在细胞中协同工作,以及它们在疾病中的作用[41][42][43][44][45][46][47][48]。
KEGG(京都基因和基因组百科全书)是一个生物信息学资源,用于从高级和基因组视角理解细胞和生物体的功能和效用[49]。KEGG的主要组成部分是PATHWAY数据库,它包含了大部分已知的代谢途径和一些已知的调控途径的生化途径图 [50]。这些途径信息也通过表示不同生物之间同源和旁系基因组的同源组表格来表示[51]。KEGG PATHWAY数据库包含了正常和扰动状态下的分子系统的途径图[52]。KEGG的目标是为了理解和模拟细胞或生物体从其基因组信息中的高级功能行为[53]。
G13通路是一种由G蛋白偶联受体(GPCRs)激活的信号传导途径。G13是异源三聚体G蛋白的一种,主要通过与GPCRs相互作用来传递信号 [54]。G13通路在多种生理过程中起着关键作用,包括细胞迁移、转化和血管平滑肌的收缩 [55][56]。此外,G13通路还可以通过激活特定的效应器,如磷脂酶D和腺苷酸环化酶7,来调节其他信号通路[57][58]。在某些情况下,G13通路的异常调节可能与人类疾病的发展有关,例如肿瘤的生长和转移[59]。
S-去甲氯胺酮
S-去甲氯胺酮是一种更强效的氯胺酮形式,医生可以以较低剂量开出具有类似效果的处方。在2019年,美国食品药品监督管理局(FDA)批准使用名为Spravato的S-去甲氯胺酮鼻喷雾治疗抗药性抑郁症[2]。
S-去甲氯胺酮的作用机制是通过与大脑中产生一种名为谷氨酸的化学物质的受体结合,从而帮助激活大脑中的谷氨酸。专家们尚未确定谷氨酸在抑郁症症状中的确切作用,但他们知道它在情绪调节中起着关键作用。大脑中谷氨酸水平低可能导致抑郁症症状。
S-去甲氯胺酮还可以刺激产生脑源性神经营养因子,这种蛋白质在神经可塑性中起作用,通过支持神经可塑性,S-去甲氯胺酮可能有助于改变导致抑郁症的负面思维模式[2]。
相比于传统的抗抑郁药,S-去甲氯胺酮的一个主要优势在于其作用非常快速。传统的抗抑郁药可能需要几周的时间才能看到症状的改善,而S-去甲氯胺酮可能在1小时内就能提供缓解 [2]。
S-去甲氯胺酮对抑郁症的治疗效果的持续时间因个体差异而异。一项研究发现,接受S-去甲氯胺酮治疗的抑郁症患者,在最后一次治疗后的中位复发时间为18天[60]。另一项研究发现,接受长期S-去甲氯胺酮输液的患者在治疗结束后的抑郁症症状改善可以持续8周[61]。然而,另一项研究指出,即使在多次治疗后,S-去甲氯胺酮的治疗效果并不会显著下降[62]。这些研究结果表明,S-去甲氯胺酮的抗抑郁效果可以持续一段时间,但具体持续时间可能因个体差异而异。
其他麻醉药物
Tramadol
曲马多(tramadol)是一种独特的镇痛药,通过在多个部位起作用,提供适度的、剂量相关的疼痛缓解。与纯阿片类受体激动剂相比,它具有较低的呼吸抑制、耐受性和依赖性风险[63]。
曲马多的作用机制是弱的mu阿片受体激动剂和血清素和去甲肾上腺素的再摄取抑制剂[64]。
曲马多可能具有抗抑郁性质。一项研究发现,曲马多在高剂量(40mg/kg,腹腔注射)时在小鼠强迫游泳试验中表现出抗抑郁样效应。NMDA受体拮抗剂(如氯胺酮、MK-801或硫酸镁)的非有效剂量与曲马多的次有效剂量(20mg/kg,腹腔注射)联合应用,可在小鼠强迫游泳试验中产生显著的抗抑郁样效应。这些数据暗示NMDA受体信号在曲马多在小鼠强迫游泳试验中的抗抑郁样效应中起作用[65]。
相比于传统的抗抑郁药,曲马多的优势在于其独特的作用机制和较低的副作用风险。然而,需要注意的是,尽管曲马多可能具有抗抑郁效果,但其主要的临床应用仍然是作为镇痛药。在使用曲马多作为抗抑郁药之前,需要进行更多的研究来确认其效果和安全性。
纯阿片类受体激动剂是一种能够与阿片受体结合并产生生理效应的药物,这些效应可以被纳洛酮这类阿片受体拮抗剂所逆转。这类药物主要用于治疗中度至重度疼痛。纯阿片类受体激动剂包括吗啡、芬太尼等。这些药物能够全面激活mu阿片受体,产生最大的药理反应。与部分阿片受体激动剂(如布洛芬)相比,纯阿片类受体激动剂在临床上可能具有更好的药效学特性,包括更有效的镇痛效果和较低的成瘾倾向[66]。
mu阿片受体激动剂是一种药物,它们能够与大脑和神经系统中的mu阿片受体结合,产生镇痛效果。这些药物包括吗啡和其他相关化合物,它们被用作治疗中度到重度疼痛的一线疗法。然而,尽管mu激动剂在疼痛管理中有明显的益处,但使用这些药物也会产生严重的副作用,如依赖性和呼吸抑制。此外,还有一些双功能的阿片受体激动剂,如AT-121,它在NOP和MOP受体上都具有部分激动剂活性,能够抑制药物的滥用效果,同时产生类似吗啡的镇痛效果,而不会引起常见的阿片类药物副作用,如呼吸抑制、滥用潜力、阿片诱导的疼痛过敏和物理依赖性[67][68]。
去甲肾上腺素,也被称为去甲肾上腺素,是大脑中的一种神经递质,对于调节警觉性、注意力、认知功能和应激反应起着重要的作用。它也作为激素在“战斗或逃跑”反应中的外周神经系统中起作用。去甲肾上腺素系统已经被暗示在一些重要的神经精神疾病的发病机制中,并且已经成为各种精神病、神经病和心肺疾病的重要药物靶点[69]。
再摄取抑制剂是一类药物,主要用于治疗抑郁症。这类药物主要通过抑制大脑中某些化学物质的再摄取来改善情绪或压力。其中,选择性5-羟色胺再摄取抑制剂(SSRIs)主要通过阻止血液从大脑吸收部分5-羟色胺,从而使大脑中的5-羟色胺水平提高,有助于缓解抑郁症[70]。另一类药物是5-羟色胺和去甲肾上腺素再摄取抑制剂(SNRIs),它们通过阻止5-羟色胺和去甲肾上腺素回到释放它们的细胞中,从而保持大脑中这两种化学信使的水平[71]。
MK-801,也被称为Dizocilpine,是一种强效的抗惊厥药,主要通过阻断N-甲基-D-天冬氨酸(NMDA)受体来发挥作用[72]。NMDA受体是一种重要的神经递质谷氨酸的受体,参与大脑中的许多重要功能,包括记忆和学习。MK-801也被发现可以抑制乙酰胆碱受体(nAChRs)[73]。此外,MK-801还被广泛用于动物研究,用于研究NMDA受体阻断对行为和记忆的影响[74]。然而,需要注意的是,MK-801的使用可能会影响记忆的编码,尤其是当药物状态在编码和记忆测试阶段发生变化时[75]。
Midazolam
咪达唑仑是一种用于治疗抑郁症的药物,其作用机制与其他抗抑郁药物不同。
咪达唑仑通过阻断α2自受体和α2异受体,直接增强去甲肾上腺素神经传输,间接增强5-HT1A介导的神经传输,因为咪达唑仑阻断了5-HT2和5-HT3受体[76][77]。
咪达唑仑的这种双重作用机制可能使其在治疗内源性抑郁症、重度抑郁症或住院抑郁症患者等难以治疗的患者群体中具有优于单一作用机制药物的疗效[78]。然而,目前尚无足够的证据表明咪达唑仑比其他抗抑郁药物更快起效。
α2自受体是一种在心脏、血管、肾脏和大脑中发挥作用的肾上腺素受体,它们通过调节神经递质的释放来调控心血管功能。α2自受体有三种亚型:α2A、α2B和α2C。α2A和α2C亚型在心脏和中枢神经系统的肾上腺素神经元中调控神经递质的释放。α2A自受体在高刺激频率下抑制递质释放,而α2C亚型在神经活动较低的水平上调节神经传输。α2B自受体的刺激会导致短暂的血管收缩。这些受体的活动对于维持心血管稳态至关重要[79][80][81]。
α2异受体是一种在心血管系统中起关键作用的腺苷酸环化酶抑制性G蛋白偶联受体。这种受体主要通过内源性儿茶酚胺(肾上腺素和去甲肾上腺素)的活化来发挥其生物学作用。α2异受体有三种亚型:α2A、α2B和α2C。α2A-受体通过中枢抗高血压作用介导α2-激动剂(如克隆尼丁和莫昔尼丁)的作用。血管α2B-受体的刺激会导致短暂的血管收缩。交感神经释放去甲肾上腺素受到前突触α2A-和α2C-受体的控制。如果α2A-和α2C-受体被删除,由于长期增强的儿茶酚胺释放,会导致心肌肥大和心力衰竭[79]。
5-HT1A是一种血清素受体,也被称为5-羟色胺1A受体。这种受体在大脑中的某些区域,如丘脑和皮质区,起着重要的作用。5-HT1A受体是血清素(5-羟色胺,5-HT)的主要受体之一,血清素是一种在大脑中发挥作用的神经递质。5-HT1A受体的激活可以抑制神经元的活动,这种抑制作用在抗抑郁和抗焦虑反应中尤其重要[82]。此外,5-HT1A受体还在调节食欲、免疫反应和炎症反应中发挥作用[83][84]。因此,5-HT1A介导的是一种通过激活5-HT1A受体来调节神经元活动和各种生理反应的过程。
违禁药物
Lysergic acid diethylamide(LSD)
麦角酸二乙胺(LSD)被发现具有抗抑郁的效果[85]。
麦角酸二乙胺,也被称为“摇头丸”或“Ecstasy”,是一种兴奋剂和致幻剂,主要通过增加突触间隙的5-羟色胺(血清素)水平来产生效果[86]。
在一些研究中,LSD显示出了抗抑郁样的效果,尤其是在有抑郁倾向的个体中,这可能是由于其增加血清素水平的作用[86][87]。
LSD的作用机制与传统的抗抑郁药物(如选择性血清素再摄取抑制剂,SSRIs)不同,SSRIs的作用是阻止血清素的再摄取,从而增加其在突触间隙的浓度,而LSD则直接增加血清素的释放[88]。
LSD的一个主要优势是其快速起效的特性,一些研究显示,LSD在短时间内就能显著改善抑郁症状,而传统的抗抑郁药物通常需要连续使用4-8周才能显现出显著的效果[89][90]。然而,需要注意的是,LSD目前仍被视为一种非法物质,其潜在的滥用风险和副作用也不能忽视[91]。
Psilocybin
骄子眼碱(psilocybin)被发现具有抗抑郁的效果[92]。
骄子眼碱是一种存在于某些种类的蘑菇中的致幻化合物,被研究用于治疗抑郁症[93]。
研究发现,psilocybin结合心理治疗可以迅速改善抑郁症症状,这与传统的抗抑郁药(如SSRIs)需要长达6周才能完全发挥效果形成鲜明对比 [93]。然而,psilocybin的具体作用机制尚不清楚,一些研究认为其抗抑郁效果可能与5-HT2AR(5-羟色胺2A受体)的激活无关[94]。
相比于传统的抗抑郁药,psilocybin的优势在于其快速起效和持久的疗效,以及与心理治疗相结合的治疗方式[95]。需要注意的是,psilocybin的研究仍处于早期阶段,其安全性和有效性需要进一步的大规模随机研究来确认[95]。
Ayahuasca
死藤水(ayahuasca)是一种由Banisteriopsis caapi藤和Psychotria viridis灌木的成分制成的酿造物,具有致幻特性[96]。Ayahuasca中的主要活性成分是精神活性色胺N,N-二甲基色胺(DMT)和单胺氧化酶抑制剂(MAOi)[97]。一项针对29名抗药性抑郁症患者的双盲随机对照试验发现,与安慰剂相比,死藤水在所有时间点上都显示出显著的抗抑郁效果[98]。
Ayahuasca在抑郁症治疗中的作用机制可能与其对正念和行为激活的影响有关。研究发现,Ayahuasca体验后的正念和行为激活的改变与抑郁症症状的减轻强烈相关[99]。Ayahuasca还可能通过激活sigma-1受体,这种蛋白质可以阻止神经退化并调节抗氧化化合物的产生,从而保护大脑细胞[96]。
相比于传统的抗抑郁药物,Ayahuasca的优势在于其快速起效的抗抑郁效果。研究表明,Ayahuasca的抗抑郁效果可以在使用后的第一天就开始显现[97]。然而,尽管Ayahuasca在临床试验中显示出相对的安全性,但其使用仍可能导致恶心、呕吐、头痛和心血管测量的短暂增加等不良事件[100]。因此,Ayahuasca的使用需要在经验丰富的治疗师的监督下进行[96]。
Banisteriopsis caapi是一种来自亚马逊盆地的木质藤蔓,被广泛用作一种神圣的饮料ayahuasca的主要成分,这种饮料在亚马逊地区的治疗和精神探索中被广泛使用。Banisteriopsis caapi含有harmine,harmaline和tetrahydroharmine等生物碱,具有抑制单胺氧化酶(MAO)的活性。这种植物的有用性已经被证明可以缓解神经系统疾病,包括帕金森病的症状[101][102]。此外,一些研究还发现Banisteriopsis caapi的生物碱可以刺激体外的成年神经发生[103]。
Psychotria viridis是一种在南美洲亚马逊盆地地区广泛分布的灌木,它是制作一种名为Ayahuasca的迷幻饮料的主要成分之一。这种植物的叶子含有一种名为N,N-二甲基色胺(DMT)的强力迷幻物质,这种物质是Ayahuasca的主要活性成分之一。Psychotria viridis的叶子还含有其他化学成分,如五环三萜类,甾体,多不饱和三萜类,醛类,长链脂肪酸等。这种植物在传统上被用作精神交流,魔法体验,治疗和宗教仪式的工具,现在也被用于民间医学和精神治疗[104][105][106][107]。
精神活性色胺,也被称为5-羟色胺或血清素,是一种单胺神经递质,对于多种复杂的生物功能起着重要的作用。它的化学名称是5-羟色胺,因此常被缩写为5-HT。血清素是由色氨酸通过羟基化(即添加-OH基团)和脱羧化形成的。血清素在人体中的浓度最高的地方是胃肠道的肠嗜铬细胞,中枢神经系统和血小板中也有少量存在。血清素通过作用于血清素受体,这些受体与不同的G蛋白耦合,从而引发细胞内的变化,影响细胞的变化。血清素在人体中的生物功能包括影响学习、记忆、快乐和奖赏,以及调节睡眠、行为和食欲等生理过程。血清素在抗抑郁药物,如SSRIs和SNRIS的药动学活动中起着重要的作用。这种化合物不仅在哺乳动物中存在,还存在于昆虫、植物和真菌中。因此,摄入这些生物可以影响人体中的血清素水平,偶尔会导致不良反应[108]。
N,N-二甲基色胺(DMT)是一种广泛存在于植物和动物中的吲哚生物碱。当人体摄入时,它能产生短暂而强烈的迷幻效果。越来越多的证据表明,内源性DMT在周围和中枢神经系统的许多过程中起着重要作用,可能作为一种神经递质。DMT的药代动力学、在周围和中枢神经系统的作用机制、临床用途和副作用都已经得到了研究。除了在大剂量静脉注射时产生强烈的心血管效应外,DMT似乎对神经系统的毒性和其他副作用有限。由于其在神经系统信号传导中的作用,DMT可能是探索大脑工作方式的有用实验工具,也可能是治疗焦虑和精神病的有用临床工具 [109]。
正念是一种注重在当下,以无判断、开放和接纳的态度去体验每一刻的过程。它源自佛教的冥想实践,但在现代被广泛应用于心理治疗和压力管理中[110][111]。正念训练可以帮助人们更好地感知情绪,降低压力感知,并更有效地应对刺激 [112]。此外,正念还可以提高人们的专注力,减少多任务处理带来的压力 [113],并可能鼓励人们参与健康的身体活动[114]。在医疗领域,正念被用作一种工具,帮助医疗专业人员和患者在危机时期,如COVID-19大流行期间,更好地管理压力[115]。
sigma-1受体是一种独特的配体调控分子伴侣,主要位于细胞的内质网中。这种受体在许多疾病中都有所涉及,包括药物成瘾、失忆、疼痛、抑郁症、阿尔茨海默病、中风、视网膜神经保护、HIV感染和癌症[116]。sigma-1受体在生物系统中的最突出作用是调节和调控电压调控和配体门控离子通道,包括Ca(2+)-, K(+)-, Na(+), Cl(-), 和SK通道,以及NMDA和IP3受体 [116]。此外,sigma-1受体在神经退行性疾病中也起着重要的作用,通过调节钙信号、线粒体功能和减少内质网应激来提供神经保护[117]。
K粉
K粉主要是盐酸氯胺酮,Ketamine Hydrochloride 直译就是克他命盐酸盐,克他命盐酸盐是一种药物,最初在1960年代被用作麻醉药。然而,医疗专业人士很快注意到,它不仅具有镇静效果,有些人在接受克他命治疗后还报告说他们的情绪有所改善。在2000年代,医疗专业人士开始研究克他命作为可能的抑郁症治疗方法[2]。
克他命盐酸盐的作用机制是通过与大脑中产生一种名为谷氨酸的化学物质的受体结合,从而帮助激活大脑中的谷氨酸。虽然专家尚未确定谷氨酸在抑郁症症状中的确切作用,但他们知道它在情绪调节中起着关键作用。大脑中谷氨酸水平低可能导致抑郁症症状。克他命还可以刺激产生脑源性神经营养因子,这种蛋白质在神经可塑性中起作用,或者说是大脑在经历新事物时的适应能力。通过支持神经可塑性,克他命可能有助于改变导致抑郁症的负面思维模式[2]。
相比于传统的抗抑郁药,克他命的一个主要优势在于其作用非常快。传统的抗抑郁药可能需要几周的时间才能看到症状的改善,而克他命可能在1小时内就能提供缓解[2]。
Dextromethorphan
右美沙芬(Dextromethorphan)是一种被称为抗咳药的药物,也是许多非处方咳嗽药物的活性成分,如Robitussin和Nyquil[118]。最近的研究发现,当与其他抗抑郁药物结合使用时,dextromethorphan可以帮助减轻抑郁症状。事实上,dextromethorphan和bupropion的组合在2022年被批准用于治疗重度抑郁症,因为在临床试验中显示出了有希望的结果[118]。
Dextromethorphan可能对抑郁症有效,因为它影响与谷氨酸相关的途径,谷氨酸是一种可能在抑郁症发展中起作用的神经递质。当与bupropion(Wellbutrin),一种常见的抗抑郁药,配对时,这种特定的药物组合显示出有帮助缓解抑郁症的希望[118]。
相比于传统的抗抑郁药,dextromethorphan/bupropion在治疗重度抑郁症(MDD)的症状方面更有效。在2022年的第三阶段临床试验中,研究人员发现dextromethorphan/bupropion比安慰剂在治疗MDD症状方面更有效,治疗的第一周就可以看到效果。此外,经过6周的治疗,超过39%的参与者能够实现MDD的缓解,而安慰剂组只有17.3%[118]。
DXM在超过推荐剂量时可能会产生一系列的心理和身体效应,这种现象被称为”Robotripping”。DXM的效应取决于剂量,例如,100-200毫克的DXM可以产生类似于摇头丸的效果,而500-1500毫克的DXM则可以产生类似于PCP的幻觉效果。DXM还可能导致一些身体效应,如增加体温、出汗、恶心、头晕、言语不清、乏力、高血压、呼吸缓慢、心跳不规则等。尽管DXM是合法的,但是用于”Robotripping”的剂量并不安全[119]。在Nuedexta这种药物中,DXM是一种活性成分,有时会被青少年滥用。
裸盖菇素
裸盖菇素是一种存在于“魔术蘑菇”中的致幻化合物,近年来在抑郁症治疗中显示出潜力。
早期研究表明,裸盖菇素能够产生快速且持久的抗抑郁效果 [120][93][121]。其作用机制尚未完全明确,但一些研究表明,裸盖菇素可能通过改变大脑中的神经传递物质,如5-羟色胺,来产生其抗抑郁效果[122]。
相比于传统的抗抑郁药物,裸盖菇素的优势在于其快速起效,传统的抗抑郁药物(如SSRIs)可能需要长达6周才能发挥全效,而裸盖菇素的抗抑郁效果几乎是立即的[93][123]。需要注意的是,裸盖菇素的使用需要在专业人员的监督下进行,并且在使用前后需要进行心理咨询[121]。
论文精读
鼻喷剂随机临床试验
这篇是 Efficacy of Esketamine Nasal Spray Plus Oral Antidepressant Treatment for Relapse Prevention in Patients With Treatment-Resistant Depression: A Randomized Clinical Trial[6],我翻译为 艾氯胺酮鼻腔喷雾剂加口服抗抑郁剂治疗对耐药抑郁症患者预防复发的疗效: 一项随机临床试验
整体看下来,这份文献更像是一份实验调查研究,最开始的摘要也没有,只有一些重要性、目的等内容。下面就让我们逐段来进行阅读。
摘要
重要性
对照研究显示,艾氯胺酮对耐药性抑郁症(TRD)具有短期疗效,但长期疗效仍有待确定。
目的
评估艾氯胺酮鼻喷雾剂加口服抗抑郁药,与安慰剂鼻腔喷雾剂加口服抗抑郁药相比。对经过艾氯胺酮鼻喷雾剂加口服抗抑郁药诱导和优化疗程后,病情稳定缓解的TRD患者,延缓抑郁症状复发的疗效。
设计、设置、参与者
这项3期、多中心、双盲、随机停药研究,于2015年10月6日至2018年2月15日在门诊转诊中心进行,共招募了705名经前瞻性确诊患有TRD的成人;455人进入优化阶段,接受艾氯胺酮鼻喷雾剂(56或84毫克)加口服抗抑郁药治疗。经过16周的艾氯胺酮治疗后,297名获得稳定缓解或稳定应答的患者进入随机停药阶段。
干预措施
获得稳定缓解的患者和获得稳定应答(无缓解)的患者按 1:1 随机分配,继续使用艾氯胺酮鼻喷雾剂或停止艾氯胺酮治疗,改用安慰剂鼻腔喷雾剂,每组患者继续口服抗抑郁药治疗。
主要结果和措施
通过加权组合对数秩检验,对获得表观缓解的患者的复发时间进行了评估。
结果
在进入随机维持治疗阶段的297名成人(平均年龄[SD],46.3 [11.13]岁;197 [66.3%]名女性)中,176人获得了稳定缓解;艾氯胺酮和抗抑郁药组有24人(26.7%)复发,抗抑郁药和安慰剂组有39人(45.3%)复发(对数秩P = .003,治疗所需人数[NNT],6)。
在获得稳定应答的121人中,艾司卡胺和抗抑郁药组有16人(25.8%)复发,抗抑郁药和安慰剂组有34人(57.6%)复发(log-rank P < .001,NNT,4)。与抗抑郁药和安慰剂治疗相比,艾司西塔明和抗抑郁药治疗可将获得稳定缓解的患者的复发风险降低51%(危险比[HR],0.49;95% CI,0.29-0.84),将获得稳定应答的患者的复发风险降低70%(HR,0.30;95% CI,0.16-0.55)。随机分组后,埃斯开他敏治疗患者最常见的不良反应是一过性呼吸困难、眩晕、解痉、嗜睡和头晕(发生率为20.4%-27.0%),每种不良反应在接受抗抑郁药和安慰剂治疗的患者中发生的比例较低(<7%)。
结论和相关性
对于经艾氯胺酮治疗后病情缓解或有反应的TRD患者,与口服抗抑郁药加安慰剂相比,在口服抗抑郁药的同时,继续使用艾氯胺酮鼻喷雾剂在延缓复发方面具有临床意义。
开头
抑郁症是导致全球残疾的主要原因,与预期寿命缩短 10 年有关。实现和维持缓解是这种反复发作疾病的治疗目标,可改善患者的功能,降低自杀风险,并提高临床稳定性。即使TRD患者对治疗有反应,在继续使用同一种抗抑郁药治疗2次(65%;3.1个月内)和3次试验失败(71.1%;3.3个月内)后,总体复发率也很高。
使用外消旋氯胺酮和立体异构体氯胺酮(esketamine)进行的几项短期研究已证明对TRD有疗效。据我们所知,这是第一项艾氯胺酮的对照维持研究,评估了间歇性使用艾氯胺酮鼻喷雾剂和口服抗抑郁药是否能比单独使用口服抗抑郁药更有效地维持TRD患者的抗抑郁效果。
方法
研究人群
患者是在2项短期双盲、活性对照研究(1项固定剂量研究和1项灵活剂量研究)中的1项研究中对艾氯胺酮鼻喷雾剂产生治疗反应(蒙哥马利-阿斯伯格抑郁量表[MADRS]总分比基线降低≥50%)后直接入组或转入本研究的,所有患者均符合相同的入组标准(报告于别处)。研究对象是正在接受治疗或转诊到美国、加拿大和欧洲的各种学术和非学术诊所的门诊患者。入选患者由其主治医生联系,或对机构审查委员会或独立伦理委员会批准的患者招募材料作出回应。此外,还开发了一种基于网络的预筛选工具,以帮助研究机构确定合适的研究候选者。
试验方案见附录 1。研究按照《赫尔辛基宣言》的伦理原则、《良好临床实践》和相关法规要求进行。所有患者在参加研究前均提供了书面知情同意书。
符合条件的患者(年龄在 18-64 岁之间)均为复发性或单次发作(≥2 年)MDD(DSM-5)17 ,临床医师评定的抑郁症状量表18 总分在 34 分或以上,MADRS 总分在 28 分或以上,表明为中度至重度抑郁。筛查时,所有患者均对当前抑郁发作中至少 1 种但不超过 5 种抗抑郁药有反应,且在前瞻性筛查阶段通过 4 周或更长时间的观察治疗证实对不同的口服抗抑郁药无反应。主要排除标准包括精神病史、前一年内的自杀行为、当前或近期的杀人或自杀意念或意图、诊断为具有精神病特征的 MDD 以及 6 个月内中度或重度药物或酒精使用障碍。有氯胺酮使用障碍史(终生)者除外。(纳入和排除标准的完整列表见补充资料 2 的电子附录 2)。尿液药物筛查(如巴比妥类药物、美沙酮、鸦片制剂、可卡因、大麻类药物、苯环利定、苯丙胺或甲基苯丙胺)在整个研究期间的用药前间歇性进行。
关键点
问题:艾氯胺酮鼻喷雾剂对耐药抑郁症患者有哪些长期影响?调查结果:在这项临床试验的维持治疗阶段,297名患有难治性抑郁症的成人接受了随机治疗。在接受了16周的埃斯卡胺和抗抑郁药的初始治疗后,那些继续接受间歇性艾氯胺酮鼻喷雾剂和口服抗抑郁药治疗的人与接受口服抗抑郁药和安慰剂鼻腔喷雾剂治疗的人相比,复发时间明显推迟。
意义:与单独口服抗抑郁药相比,艾氯胺酮鼻喷雾剂加抗抑郁药的持续治疗可在更大程度上维持耐药抑郁症患者的抗抑郁效果。
研究设计
这项双盲、随机临床试验(成人难治性抑郁症患者鼻内注射依斯西塔明加口服抗抑郁药预防复发的研究[SUSTAIN-1])采用随机戒断设计,于2015年10月6日至2018年2月15日进行,共有99个研究点对患者进行了随机试验。
研究最多包括 5 个阶段:
- (1) 4 周筛选和前瞻性观察阶段(仅限直接入组患者)
- (2) 4 周开放标签诱导阶段(仅限直接入组患者)
- (3) 12 周优化阶段(开放标签、直接入组患者或双盲、转移入组患者)
- (4) 维持阶段(双盲、随机停药、事件驱动、持续时间不定)
- (5) 2 周治疗后随访阶段。研究一直持续到达到计划中期分析(如下所述)规定的复发次数为止。
直接入院患者
在为期 4 周的筛查和观察阶段,对符合条件的患者进行持续口服抗抑郁药治疗无应答前瞻性评估。在这一阶段结束时无应答的患者将停用之前的抗抑郁药,并可选择为期3周或更短的减量期。在诱导阶段,患者接受艾司卡胺鼻腔喷雾剂(56 或 84 毫克,剂量灵活)治疗,每周两次,同时每天口服一种新的抗抑郁药物(度洛西汀、艾司西酞普兰、舍曲林或缓释文拉法辛)。
转院入院和直接入院患者
在诱导阶段结束时获得治疗应答(即MADRS评分比基线降低≥50%)的转入患者和直接进入患者进入为期12周的优化阶段,在此期间,诱导阶段结束时的研究药物剂量保持不变,但鼻内给药频率减少为每周一次,持续4周,然后根据抑郁症状的严重程度个性化为每周或每两周一次。为了保持盲法,转入患者继续接受诱导阶段的治疗任务(艾氯胺酮或安慰剂)。
维护阶段
在优化阶段的第16周,经艾司卡胺治疗的直接入组(开放标签治疗)和转移入组(双盲治疗)患者达到稳定缓解(主要分析集; 定义为最近 4 周中有 3 周 MADRS 评分≤12 分,仅允许在第 13 周或第 14 周出现 1 次偏离[MADRS 评分 >12 分]或缺失 1 次 MADRS 评估)和具有稳定应答的患者(次要分析组;定义为在优化阶段的最后 2 周,MADRS 评分比基线降低≥50%,但未达到缓解)继续进入维持阶段。据报道,与有反应但未缓解的患者相比,获得缓解的耐药患者的复发率较低3 ,因此预设的主要分析是对获得稳定缓解的患者进行分析。
不过,符合不太保守的稳定应答(但非稳定缓解)标准的患者也接受了评估,因为在这一患者群体中,MADRS评分与基线相比连续两周下降50%或以上被认为是有临床意义的。获得稳定缓解的患者和获得稳定应答(无缓解)的患者按照计算机生成的时间表以1:1的比例分别随机分配,继续接受艾氯胺酮治疗或停止艾氯胺酮治疗并改用安慰剂鼻腔喷雾剂,每种治疗方法均在口服抗抑郁药治疗的基础上进行。在整个维持治疗阶段,抗抑郁药的剂量与诱导治疗阶段相同。随机化采用随机排列的区块进行平衡,并按国家进行分层。
在短期研究中被分配到抗抑郁剂组和安慰剂组并获得稳定缓解或稳定应答的转入患者,在维持治疗阶段继续接受相同的治疗,并被纳入本研究的安全性分析,但不包括疗效分析。
符合复发标准的患者可继续接受长期的艾氯胺酮鼻喷雾剂维持治疗研究。
鼻内研究药物和管理
埃斯氯胺酮和安慰剂均装在鼻腔喷雾装置中,每个装置各含 200 μL 溶液(即 2 次喷雾)。每个装置含有 32.28 毫克盐酸埃斯氯胺酮(28 毫克埃斯氯胺酮碱)或安慰剂。安慰剂溶液含有苦味剂(苯甲酸地那铵),以模拟埃斯卡他敏溶液的味道并保持盲法。
功效评估
在整个研究过程中(筛选和观察阶段的第 1、2 和 4 周,以及诱导、优化、维持和随访阶段的每周),由独立的远程盲法评分员进行 MADRS 评估。
安全评估
在整个研究过程中监测不良事件 (AE) 和其他安全性评估,包括临床实验室检查、体格检查、心电图、哥伦比亚自杀严重程度评定量表 (C-SSRS)(0 表示无自杀意念或行为;1-5 表示有自杀意念;6-10 表示有自杀行为;项目描述见补充资料 2 中的电子附录 3)。在基线和所有治疗用药访视时(用药前、用药后 40 分钟、1 小时(仅限生命体征)和 1.5 小时),对生命体征、临床医师管理的分离状态量表 (CADSS) 和简明精神病评定量表(4 项阳性症状分量表)进行评估。
研究人员采用了 20 项医师戒断检查表来评估停止鼻内注射研究药物后可能出现的戒断症状。用药前进行了认知测试,以评估对认知的潜在影响;这些数据将在另一篇文章中报告。
统计分析
样本量的确定
根据假设(应计期和应计率、最长研究持续时间和辍学率),需要对211名获得稳定缓解的患者进行随机分组(1:1比例),以获得84例复发病例,在双侧α为0.05的固定样本设计下,90%的功率可检测出危险比(HR)为0 49,从而检测出艾司卡胺和抗抑郁药在延迟复发方面优于抗抑郁药和安慰剂。在对获得稳定缓解的患者进行分析时,采用了两阶段分组序列设计,独立的数据监测委员会在31次复发后进行了预先指定的中期分析,以评估早期疗效。
对获得稳定缓解的患者进行的中期分析并未显示艾氯胺酮和抗抑郁药优于抗抑郁药和安慰剂(双侧显着性水平为 0.0097,对数秩检验); 因此,研究继续进行,并且将获得稳定缓解的患者的复发人数重新估计为总共 59 例复发,最终疗效分析的显着性水平调整为 0.046(两侧)(基于 Wang-Tsiatis 边界) α-支出函数24),确保中期分析后的条件功效达到90%或更高。
功效终点和分析
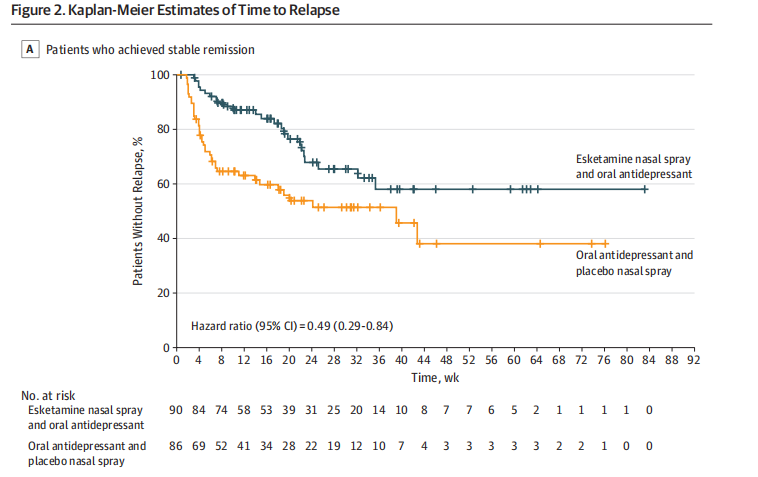
通过 Kaplan-Meier 方法估计达到稳定缓解(主要疗效终点)的患者和达到稳定缓解但未缓解(次要终点)的患者之间维持阶段复发时间的累积分布。 复发被定义为相隔 5 至 15 天的 2 次连续评估,MADRS 总分达到 22 分或更高,或因抑郁症恶化、自杀未遂、自杀预防或自杀完成而住院,或提示复发的其他临床相关事件(通过复发评估) 评审委员会)。
使用对数秩检验分析组间复发时间差异(对因进行中期分析而获得稳定缓解的患者进行加权组合[中期和最终分析])。 估计的 HR 和 95% CI 基于实现稳定缓解的患者的加权估计以及以治疗作为实现稳定缓解的患者的因素的 Cox 比例风险回归模型。 结合获得稳定缓解的患者分析组和获得稳定缓解的患者分析组进行了类似的事后分析。
结果
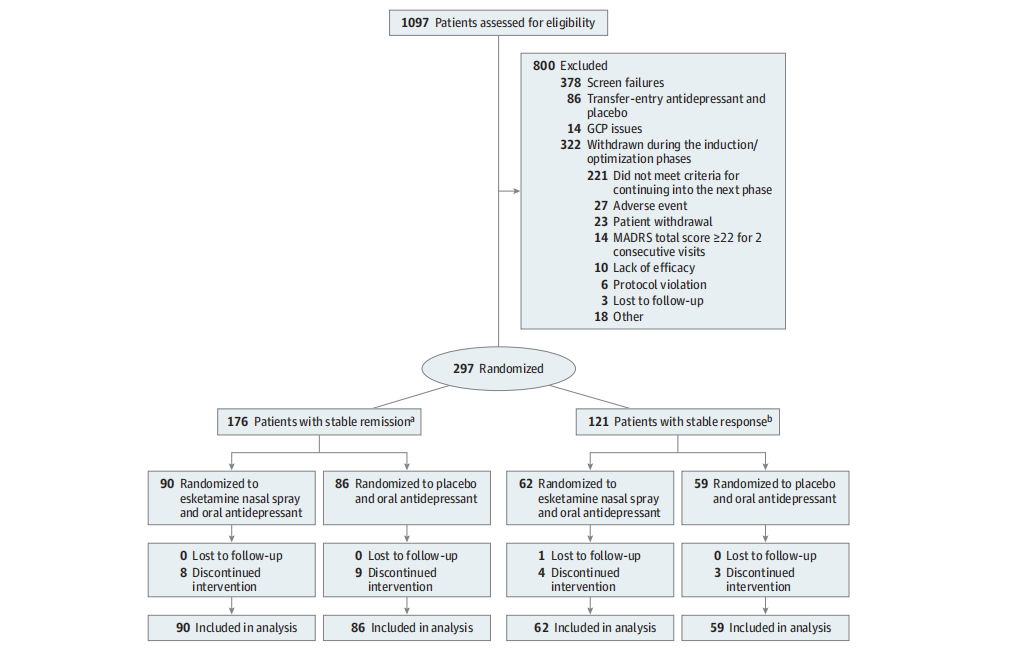
共有 297 名成年人(平均年龄 [SD],46.3 [11.13] 岁;197 名 [66.3%] 女性)被随机分配到研究的维持阶段。 CONSORT 图如图 1 所示。每个站点的患者中位数为 2 人(范围为 1-25)。 根据人口统计学和基线临床特征,治疗组具有可比性(表 1)。 在维持阶段,获得稳定缓解的患者中鼻内艾氯胺酮暴露时间的中位时间为 17.7 周,而获得稳定缓解的患者中暴露于鼻内艾氯胺酮的中位时间为 19.4 周。 获得稳定缓解的患者在维持阶段接受安慰剂的中位时间为 10.2 周,而获得稳定缓解的患者则为 10.1 周。
在艾氯胺酮联合抗抑郁药组中获得稳定缓解的 90 名患者中,40 名(44.4%)在维持期第 1 天接受了 56 毫克艾氯胺酮,50 名(55.6%)接受了 84 毫克,其中 62 名(68.9%)接受了治疗 大部分维护阶段每两周一次。 在艾氯胺酮和抗抑郁药组中获得稳定反应的 62 名患者中,较大比例在维持阶段接受了较高的艾氯胺酮剂量(56 mg:n = 20 [32.3%];84 mg:n = 42 [67.7%]), 34 名 (54.8%) 大部分时间每周接受一次治疗。
本研究使用的数据是那些接受艾氯胺酮鼻喷雾剂加口服抗抑郁药治疗 16 周的患者,在满足稳定缓解(主要分析)或稳定反应(二次分析)标准后,被随机(单独) 继续使用艾氯胺酮鼻喷雾剂加口服抗抑郁药治疗,或停止艾氯胺酮鼻喷雾剂治疗并改用安慰剂鼻喷雾剂并继续使用口服抗抑郁药。 稳定缓解被定义为蒙哥马利-阿斯伯格抑郁评定量表 (MADRS) 总分在优化阶段的最后 4 周中连续 3 周或以上为 12 或更低,最多有 1 次偏差(MADRS 总分 >12)或 1 次缺失 仅允许在第 13 周或第 14 周进行 MADRS 评估。 稳定缓解定义为在优化阶段的最后两周内,MADRS 总分较基线降低 50% 或更多,但未达到稳定缓解标准。 随机分组后失访或停止治疗的患者被纳入分析。
a.一名具有稳定缓解的患者被错误地分配到具有稳定缓解的组中。
b.一名在优化阶段结束时未达到稳定缓解或稳定反应标准的患者被错误地分配到稳定反应组中。
缩写:MADRS,蒙哥马利-阿斯伯格抑郁量表; MDD,重度抑郁症; PHQ-9,患者健康调查问卷 9; SNRI,5-羟色胺-去甲肾上腺素再摄取抑制剂; SSRI,选择性血清素再摄取抑制剂。
a.除非另有说明,数据以患者数量(百分比)表示。
b.达到稳定缓解的患者:艾氯胺酮鼻喷雾剂+口服抗抑郁药组54例,口服抗抑郁药+安慰剂鼻喷雾剂组56例; 达到稳定反应的患者:使用艾氯胺酮鼻喷雾剂和口服抗抑郁药的患者为 31 例,口服抗抑郁药和安慰剂鼻喷雾剂的患者为 41 例。
c.达到稳定缓解的患者:艾氯胺酮鼻喷雾剂+口服抗抑郁药组36例,口服抗抑郁药+安慰剂鼻喷雾剂组30例; 达到稳定反应的患者:使用艾氯胺酮鼻喷雾剂和口服抗抑郁药的患者为 31 例,使用口服抗抑郁药和安慰剂鼻喷雾剂的患者为 18 例.
d.在优化阶段和随机化之前。
e.3001 表示从 Janssen 赞助的固定剂量艾氯胺酮研究 TRD3001 转移而来。
f.3002 表示从 Janssen 赞助的灵活剂量艾氯胺酮研究 TRD3002 转移而来。
功效结果
总体而言,在获得稳定缓解的患者中,艾氯胺酮和抗抑郁药组中有 24 名患者(26.7%)以及抗抑郁药和安慰剂组有 39 名患者(45.3%)在维持阶段经历了复发事件; 在获得稳定缓解(但未缓解)的患者中,艾氯胺酮和抗抑郁药组有 16 名患者(25.8%),抗抑郁药和安慰剂组有 34 名患者(57.6%)出现复发。 与抗抑郁药和安慰剂治疗相比,继续使用艾氯胺酮和抗抑郁药治疗可显着延迟复发(达到稳定缓解的患者:HR,0.49;95% CI,0.29-0.84;P = 0.003,需要治疗的人数 [NNT],6; 达到稳定缓解的患者:HR,0.30;95% CI,0.16-0.55:P < .001,NNT,4)。 根据 HR 估计,与抗抑郁药和安慰剂相比,艾氯胺酮和抗抑郁药治疗可将获得稳定缓解的患者的复发风险降低 51%,将获得稳定缓解的患者的复发风险降低 70%。 此外,在事后分析中,在获得稳定缓解的患者和获得稳定缓解的患者中,与抗抑郁药和安慰剂相比,艾氯胺酮和抗抑郁药可延迟复发(HR,0.38;95% CI,0.26-0.57;P < .001) 。 在主要终点的事后敏感性分析中,使用 MADRS 评分截止值 10 作为缓解,组间差异仍然具有统计学显着性(双侧 P = .005)(补充 2 中的 eTable 1)。 获得稳定缓解的患者的复发时间也通过研究入组(直接与转移)进行评估。直接入组患者的 HR 为 0.49(95% CI,0.27-0.90),HR 为 0.45(95% CI,0.17-1.18) 对于转入患者。
鉴于每个中心的患者中位数较低(2;范围,1-25),为了进一步评估中心对治疗效果(即 HR)估计的影响,使用 Cox 比例风险回归进行了事后敏感性分析 通过一次排除一个站点来建立模型。 根据此分析,HR 估计范围为 0.42 至 0.57,这与整体 HR 0.47(未加权)一致。
在获得稳定缓解并改用安慰剂鼻喷雾剂的 39 例患者中,有 19 例发生在停止艾氯胺酮治疗后的第一个月(6 例在第 2 周,其余在第 4 周),其中 11 例发生在这 19 例早期复发中 在随机化前优化阶段的最后 4 周内需要每周进行治疗的患者。
完成诱导和优化治疗(总共 16 周)后,在获得稳定缓解的患者和获得稳定缓解的患者中,随机继续与停止艾氯胺酮治疗的患者之间的 MADRS 总分存在差异,每种患者均接受抗抑郁治疗, 随着时间的推移,接受艾氯胺酮治疗的患者的 MADRS 总分较低。 在获得稳定缓解的患者和获得稳定缓解的患者中都保持了这种分离。补充 2 中的 eFigure 2 显示了在诱导、优化和维持阶段使用最后观察结转数据随时间变化的平均 MADRS 总分。
缩写:HR,风险比; NE,不可估量。
a.对研究结束时保持无复发的患者进行审查,定义为达到复发事件的目标数量,或者在维持阶段提前退出且没有复发的患者。 大多数被审查的患者(即,当参与结束时)被认为是基于研究已达到终点(即,基于已实现的复发事件的目标数量并且研究停止)进行管理的。 艾氯胺酮鼻喷雾剂和口服抗抑郁药组仅有 13 例(8 名患者获得稳定缓解,5 名患者获得稳定缓解),而口服抗抑郁药和安慰剂组只有 12 例(9 名患者获得稳定缓解,3 名患者获得稳定缓解) 被审查是因为他们在复发之前和研究结束之前停止了维持阶段。数据基于 Kaplan-Meier 产品限制估计。
b.HR 和 CI 是基于 Wassmer 的加权估计,并使用 R 中的 gsDesign 和 mvtnorm 包计算。
c.双边 P 值基于最终检验统计量,该统计量是在中期和最终分析集上计算的对数秩检验统计量的加权组合。
d.基于以治疗为因素的Cox比例风险回归模型对生存数据进行回归分析。
e.对数秩检验。
安全结果
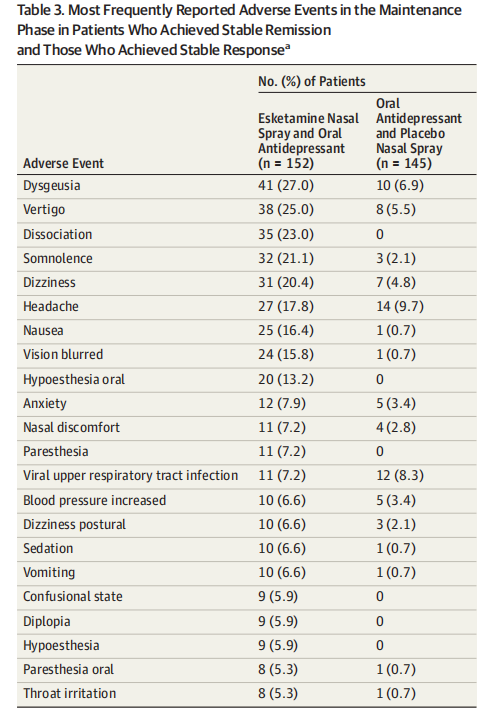
艾氯胺酮和镇潮剂组在维持阶段报告的 5 种最常见 AE 是味觉障碍、眩晕、解离、嗜睡和头晕(表 3)。 大多数 AE 为轻度至中度,在给药后观察到,并且通常在当天解决。 没有观察到呼吸抑制或间质性膀胱炎的病例。
研究期间没有死亡报告。 艾氯胺酮和抗抑郁药组中的 6 名患者报告了研究者认为与研究药物相关的严重不良事件(自主神经系统失衡、迷失方向、体温过低、腔隙性中风[即缺血性病变,给药后第 1 天、6 小时]、镇静 、简单部分性癫痫发作[第5天,给药后45分钟;无癫痫病史]和自杀意念)在诱导阶段。 在优化或维护阶段,没有报告与艾氯胺酮相关的严重不良事件。
7 名患者在维持阶段出现 1 次或以上 AE,导致停止鼻内研究药物; 152 名患者中,有 4 名 (2.6%) 属于艾氯胺酮和抗抑郁药组(抑郁症恶化,3 名患者;焦虑和精神错乱状态 [短暂],1 名患者),145 名患者中有 3 名 (2.1%) 属于抗抑郁药和安慰剂组(抑郁症恶化) 对于每个)。
在治疗日使用艾氯胺酮观察到短暂的血压升高; 在大多数情况下,在开始给药后 40 分钟达到最大值,并且通常在给药后 1.5 小时恢复到给药前范围(补充 2 中的图 3)。 很少有患者经历治疗引起的短暂性高血压,定义为收缩压 180 mm Hg 或更高和/或舒张压 110 mm Hg 或更高(即收缩性高血压:1 [0.7%] 接受艾氯胺酮治疗的患者和 0 名接受抗抑郁药和安慰剂治疗的患者;舒张期高血压:2 名 [1.3%] 接受艾氯胺酮治疗的患者和 0 名接受抗抑郁药和安慰剂治疗的患者)在维持阶段。 研究期间未观察到心电图结果有临床显着变化。
大多数直接入院患者 (362 [85.4%]) 的基线 C-SSRS 评分为 0,表明没有自杀意念或行为。 在接受艾氯胺酮和口服抗抑郁药治疗且基线时没有自杀意念或行为的患者中,42 名 (11.6%) 的基线后评分较高(最大 C-SSRS 评分为 1 [n = 35]、2 [n = 3]、 3 [n = 2]、5 [n = 1] 和 8 [n = 1])在开放标签诱导阶段; 22 名 (5.7%)(直接入院和转入患者)在基线后评分较高(最大 C-SSRS 评分为 1 [n = 17]、2 [n = 3] 和 3 [n = 2]) 优化阶段; 与接受抗抑郁药和安慰剂的 6 名患者 (4.5%) 相比,其中 3 名患者 (2.4%) 的基线后评分更高(最大 C-SSRS 评分为 1 [n = 2] 和 4 [n = 1])(最大 C-SSRS 评分 1 [n = 6])在维护阶段。 在C-SSRS的基础上,在优化或维护阶段没有自杀行为的报告。 经历复发的患者中没有一个患者的 C-SSRS 评分显着升高(即,在艾氯胺酮和抗抑郁药组中经历复发的患者中最严重的基线后评分为 2,在抗抑郁药和安慰剂组中经历复发的患者中最严重的基线后评分为 3 )。
通过 CADSS 测量,目前状态的解离症状(补充 2 中的 e 图 4)在艾氯胺酮治疗开始后不久就开始出现,在 40 分钟时达到峰值,通常在 1.5 小时内消失。 在诱导阶段,随着时间的推移重复给药,症状的严重程度会减弱,在优化和维持阶段报告的症状程度相对较低。 没有观察到精神病症状或不良事件。
值得注意的是,1 名患者在研究期间接受了 1 剂氯胺酮(10 毫克静脉注射)治疗肾结石 AE,但任何参与者均未报告与使用或滥用氯胺酮相关的 AE。 根据 20 项医师戒断检查表的评估,在停止使用艾氯胺酮鼻喷雾剂后 2 周内,没有观察到明显戒断综合征的证据。
一名获得稳定缓解的患者被错误地随机分配为在优化阶段结束时获得稳定缓解的患者。 一名患者不符合稳定缓解或稳定反应标准,并被错误地随机分配为具有稳定反应的患者。 审查参与者的最常见原因是研究结束时没有复发(参见表 2 图例)。 垂直线表示经过审查的观察结果。
a.Adverse events are listed in decreasing order based on incidence within the esketamine plus antidepressant group and in alphabetical order for events with the same incidence. The incidence was 5% or greater in either treatment group
讨论
据我们所知,在第一项研究中,艾氯胺酮鼻喷雾剂用于预防 TRD 患者复发,持续使用艾氯胺酮和抗抑郁药治疗,与抗抑郁药和安慰剂相比,在延迟已获得稳定缓解的患者复发方面具有临床意义和统计学显着优势。 或使用艾氯胺酮和抗抑郁药治疗 16 周后出现稳定反应。 直接进入或转移进入状态在疗效上没有发现重大差异。
在解释随机戒断研究时经常提到的一个问题是,转用安慰剂后观察到的抑郁症发生率增加是抗抑郁药戒断的药理学后果。戒断早期的高复发率可能表明可能存在戒断或反弹效应。 在这项研究中,尽管改用安慰剂鼻喷雾剂的患者在第一个月内复发率很高,但鉴于艾氯胺酮血浆浓度在最初 2 至 4 小时内迅速下降,药物戒断效应不太可能起作用。 此后更加缓慢(平均终末半衰期为 7-12 小时),间歇给药从未达到稳定状态。 此外,这种高早期复发率与停止电休克治疗后观察到的相似。电休克治疗停止后没有已知的反弹效应。 艾氯胺酮停药后早期复发率很高,以及 Rush 等人在缓解抑郁的序贯治疗替代方案 (STAR*D) 研究中观察到的 3 级或 4 级患者(即先前 2 次和 3 次抗抑郁治疗失败)的早期复发率, 分别)更有可能反映 TRD 患者在单独使用抗抑郁药维持治疗期间更容易复发。
考虑到个体差异,基于 MADRS 的治疗算法将给药频率个体化为维持缓解或缓解的最低频率。如果患者达到缓解(即 MADRS 评分≤12),则给药频率减少至每 2 周一次,而无法缓解的患者则将给药频率降低至每 2 周一次。 达到或维持缓解被分配为每周给药频率。 值得注意的是,超过一半在停止艾氯胺酮治疗后第一个月内出现复发的患者需要每周给药以维持缓解,反映出该亚群的脆弱性较高。 总而言之,证据表明,停止艾氯胺酮治疗后最初几周出现的复发可能是由于患者更脆弱,而不是戒断或反弹现象。
在这项每周或每两周施用艾氯胺酮鼻喷雾剂的长期研究中,没有观察到新的或意外的安全问题。 结果与之前已完成的短期(4 周)2 期和 3 期研究的结果一致
局限性
研究的局限性包括艾氯胺酮具有已知的短暂解离和镇静作用,难以致盲; 这些症状可能会让观察治疗的工作人员产生偏见。 为了确保疗效评估的公正性,独立、远程、盲法 MADRS 评估者在整个研究过程中评估了治疗反应。 此外,一项事后分析评估了随机停止鼻内艾氯胺酮治疗的参与者,这些参与者随后在维持阶段的前 4 周内复发(n = 19)。 通过审查经历复发并显示随机化前后 CADSS 评分有明显变化的患者 (n = 3) 进行敏感性分析,结果 HR 为 0.50(95% CI,0.30-0.84),双侧 P = .008(与主要分析一致),基于未加权的 Cox 比例风险回归模型和对数秩检验。
结论
这项研究表明,在初始治疗 16 周后,与抗抑郁药加安慰剂相比,继续使用艾氯胺酮联合抗抑郁药治疗在预防 TRD 患者复发方面具有显着的、有临床意义的优越性,并提供了进一步的安全性数据,支持积极的获益风险比 的长期治疗。
References:
- Emerging evidence for antidepressant actions of anesthetic agents:https://pubmed.ncbi.nlm.nih.gov/29794854/
- What to Know About Ketamine Therapy for Depression:https://www.healthline.com/health/depression/ketamine-depression-treatment
- Efficacy and Safety of Intranasal Esketamine in Treatment-Resistant Depression in Adults: A Systematic Review:https://pubmed.ncbi.nlm.nih.gov/34447651/
- FDA-Approved Ketamine Nasal Spray Cuts Depression Symptoms in 24 Hours:https://www.healthline.com/health-news/ketamine-nasal-spray-can-help-reduce-depression-in-24-hours
- Benefit-Risk Assessment of Esketamine Nasal Spray vs. Placebo in Treatment-Resistant Depression:https://pubmed.ncbi.nlm.nih.gov/32860422/
- Efficacy of Esketamine Nasal Spray Plus Oral Antidepressant Treatment for Relapse Prevention in Patients With Treatment-Resistant Depression: A Randomized Clinical Trial:https://pubmed.ncbi.nlm.nih.gov/31166571/
- All About Spravato:https://www.healthline.com/health/drugs/spravato#drug-images
- Understanding Ketamine’s Use in Physical and Mental Health:https://www.healthline.com/health/mental-health/what-is-ketamine
- Drug Metabolism:https://pubmed.ncbi.nlm.nih.gov/28723052/
- The history of Ephedra (ma-huang):https://pubmed.ncbi.nlm.nih.gov/21365072/
- Ephedra (Ma Huang): Weight Loss, Dangers, and Legal Status:https://www.healthline.com/nutrition/ephedra-sinica
- Recent developments in nitric oxide donor drugs:https://pubmed.ncbi.nlm.nih.gov/17401442/
- Nitric oxide and major depression:https://pubmed.ncbi.nlm.nih.gov/21335097/
- Nitric Oxide Synthase Inhibitors as Antidepressants:https://pubmed.ncbi.nlm.nih.gov/27713253/
- Ketamine and nitrous oxide: The evolution of NMDA receptor antagonists as antidepressant agents:https://pubmed.ncbi.nlm.nih.gov/32240970/
- Rapid recovery from major depression using magnesium treatment:https://pubmed.ncbi.nlm.nih.gov/16542786/
- Antidepressant and neurocognitive effects of isoflurane anesthesia versus electroconvulsive therapy in refractory depression:https://pubmed.ncbi.nlm.nih.gov/23922809/
- Emerging evidence for antidepressant actions of anesthetic agents:https://pubmed.ncbi.nlm.nih.gov/29794854/
- Antidepressant and neurocognitive effects of isoflurane anesthesia versus electroconvulsive therapy in refractory depression:https://pubmed.ncbi.nlm.nih.gov/23922809/
- Isoflurane narcotherapy in depressive patients refractory to conventional antidepressant drug treatment. A double-blind comparison with electroconvulsive treatment:https://pubmed.ncbi.nlm.nih.gov/7659199/
- Electroconvulsive therapy and its different indications:https://pubmed.ncbi.nlm.nih.gov/18472488/
- Electroconvulsive Therapy: Mechanisms of Action, Clinical Considerations, and Future Directions:https://pubmed.ncbi.nlm.nih.gov/37171471/
- Propofol for ECT anesthesia a review of the literature:https://pubmed.ncbi.nlm.nih.gov/24820943/
- Antidepressant Efficacy and Tolerability of Ketamine and Esketamine: A Critical Review:https://pubmed.ncbi.nlm.nih.gov/29736744/
- Eukaryotic elongation factor 2 kinase, an unusual enzyme with multiple roles:https://pubmed.ncbi.nlm.nih.gov/24853390/
- Overview of protein phosphorylation:https://pubmed.ncbi.nlm.nih.gov/18228324/
- The regulation of protein phosphorylation:https://pubmed.ncbi.nlm.nih.gov/19614568/
- Myogenic signaling of phosphatidylinositol 3-kinase requires the serine-threonine kinase Akt/protein kinase B:https://pubmed.ncbi.nlm.nih.gov/10051597/
- The mammalian target of rapamycin-signaling pathway in regulating metabolism and growth:https://pubmed.ncbi.nlm.nih.gov/17998426/
- Mammalian target of rapamycin (mTOR) as a potential therapeutic target in various diseases:https://pubmed.ncbi.nlm.nih.gov/28417246/
- Mammalian target of rapamycin signaling in cardiac physiology and disease:https://pubmed.ncbi.nlm.nih.gov/24481845/
- Mammalian Target of Rapamycin (mTOR) Signalling Pathway a Potential Target for Cancer Intervention: a Short Overview:https://pubmed.ncbi.nlm.nih.gov/36999689/
- Risks Associated with Misuse of Ketamine as a Rapid-Acting Antidepressant:https://pubmed.ncbi.nlm.nih.gov/27878517/
- Microglial ERK-NRBP1-CREB-BDNF signaling in sustained antidepressant actions of (R)-ketamine:https://pubmed.ncbi.nlm.nih.gov/34819637/
- A bibliometric analysis of research on (R)-ketamine from 2002 to 2021:https://pubmed.ncbi.nlm.nih.gov/35948160/
- cAMP Response Element-Binding Protein (CREB): A Possible Signaling Molecule Link in the Pathophysiology of Schizophrenia:https://pubmed.ncbi.nlm.nih.gov/30214393/
- Mechanism of Antidepressant Action of (2R,6R)-6-Hydroxynorketamine (HNK) and Its Compounds: Insights from Proteomic Analysis:https://pubmed.ncbi.nlm.nih.gov/37632679/
- Esketamine: a glimmer of hope in treatment-resistant depression:https://pubmed.ncbi.nlm.nih.gov/31745646/
- The human natural killer-1 (HNK-1) glycan mimetic ursolic acid promotes functional recovery after spinal cord injury in mouse:https://pubmed.ncbi.nlm.nih.gov/29567576/
- Honokiol inhibits breast cancer cell metastasis by blocking EMT through modulation of Snail/Slug protein translation:https://pubmed.ncbi.nlm.nih.gov/31235819/
- GO-Elite: a flexible solution for pathway and ontology over-representation:https://pubmed.ncbi.nlm.nih.gov/22743224/
- Automated exploration of gene ontology term and pathway networks with ClueGO-REST:https://pubmed.ncbi.nlm.nih.gov/30847467/
- Integrating GO and KEGG terms to characterize and predict acute myeloid leukemia-related genes:https://pubmed.ncbi.nlm.nih.gov/25343280/
- ClueGO: a Cytoscape plug-in to decipher functionally grouped gene ontology and pathway annotation networks:https://pubmed.ncbi.nlm.nih.gov/19237447/
- Biochemical Pathways Represented by Gene Ontology Causal Activity Models Identify Distinct Phenotypes Resulting from Mutations in Pathways:https://pubmed.ncbi.nlm.nih.gov/37293039/
- Prediction and analysis of essential genes using the enrichments of gene ontology and KEGG pathways:https://pubmed.ncbi.nlm.nih.gov/28873455/
- Gene expression profiles and pathway enrichment analysis to identification of differentially expressed gene and signaling pathways in epithelial ovarian cancer based on high-throughput RNA-seq data:https://pubmed.ncbi.nlm.nih.gov/34839022/
- IL6-mediated HCoV-host interactome regulatory network and GO/Pathway enrichment analysis:https://pubmed.ncbi.nlm.nih.gov/32997660/
- Using the KEGG database resource:https://pubmed.ncbi.nlm.nih.gov/22700311/
- KEGG: Kyoto Encyclopedia of Genes and Genomes:https://pubmed.ncbi.nlm.nih.gov/9847135/
- KEGG: kyoto encyclopedia of genes and genomes:https://pubmed.ncbi.nlm.nih.gov/10592173/
- KEGG for representation and analysis of molecular networks involving diseases and drugs:https://pubmed.ncbi.nlm.nih.gov/19880382/
- The KEGG database:https://pubmed.ncbi.nlm.nih.gov/12539951/
- Signaling mechanisms and physiological functions of G-protein Gα13 in blood vessel formation, bone homeostasis, and cancer:https://pubmed.ncbi.nlm.nih.gov/30345641/
- Regulation and physiological functions of G12/13-mediated signaling pathways:https://pubmed.ncbi.nlm.nih.gov/19212140/
- G12-G13-LARG-mediated signaling in vascular smooth muscle is required for salt-induced hypertension:https://pubmed.ncbi.nlm.nih.gov/18084302/
- The alpha-subunit of the heterotrimeric G protein G13 activates a phospholipase D isozyme by a pathway requiring Rho family GTPases:https://pubmed.ncbi.nlm.nih.gov/9478920/
- Regulation of cAMP responses by the G12/13 pathway converges on adenylyl cyclase VII:https://pubmed.ncbi.nlm.nih.gov/18541530/
- GNA13 promotes tumor growth and angiogenesis by upregulating CXC chemokines via the NF-κB signaling pathway in colorectal cancer cells:https://pubmed.ncbi.nlm.nih.gov/30267476/
- Rapid and longer-term antidepressant effects of repeated ketamine infusions in treatment-resistant major depression:https://pubmed.ncbi.nlm.nih.gov/22840761/
- Prolonged ketamine infusion modulates limbic connectivity and induces sustained remission of treatment-resistant depression:https://pubmed.ncbi.nlm.nih.gov/33483802/
- Real-world effectiveness of ketamine in treatment-resistant depression: A systematic review & meta-analysis:https://pubmed.ncbi.nlm.nih.gov/35688035/
- Tramadol today:https://pubmed.ncbi.nlm.nih.gov/17016341/
- Tramadol: does it have a role in emergency medicine?:https://pubmed.ncbi.nlm.nih.gov/15675908/
- Involvement of NMDA receptors in the antidepressant-like effect of tramadol in the mouse forced swimming test:https://pubmed.ncbi.nlm.nih.gov/28754288/
- Partial versus full agonists for opioid-mediated analgesia—focus on fentanyl and buprenorphine:https://pubmed.ncbi.nlm.nih.gov/12461829/
- Mu opioid receptor antagonists: recent developments:https://pubmed.ncbi.nlm.nih.gov/17918759/
- A bifunctional nociceptin and mu opioid receptor agonist is analgesic without opioid side effects in nonhuman primates:https://pubmed.ncbi.nlm.nih.gov/30158150/
- Physiology, Noradrenergic Synapse:https://pubmed.ncbi.nlm.nih.gov/31082021/
- Selective Serotonin Reuptake Inhibitors (SSRIs): What to Know:https://www.healthline.com/health/depression/selective-serotonin-reuptake-inhibitors-ssris
- Serotonin-Norepinephrine Reuptake Inhibitors (SNRIs):https://www.healthline.com/health/depression/serotonin-norepinephrine-reuptake-inhibitors-snris
- The anticonvulsant MK-801 is a potent N-methyl-D-aspartate antagonist:https://pubmed.ncbi.nlm.nih.gov/3529096/
- MK-801 inhibition of nicotinic acetylcholine receptor channels:https://pubmed.ncbi.nlm.nih.gov/1715611/
- Evaluation of brain pharmacokinetics of (+)MK-801 in relation to behaviour:https://pubmed.ncbi.nlm.nih.gov/21871531/
- The NMDA receptor antagonist MK-801 fails to impair long-term recognition memory in mice when the state-dependency of memory is controlled:https://pubmed.ncbi.nlm.nih.gov/30902736/
- Review of the use of mirtazapine in the treatment of depression:https://pubmed.ncbi.nlm.nih.gov/21644844/
- SNaRIs, NaSSAs, and NaRIs: new agents for the treatment of depression:https://pubmed.ncbi.nlm.nih.gov/10752718/
- Mirtazapine: clinical overview:https://pubmed.ncbi.nlm.nih.gov/10446735/
- The alpha 2-adrenergic receptors: molecular structure and in vivo function:https://pubmed.ncbi.nlm.nih.gov/11677796/
- Two functionally distinct alpha2-adrenergic receptors regulate sympathetic neurotransmission:https://pubmed.ncbi.nlm.nih.gov/10647009/
- Alpha(2)-adrenergic receptor signalling in hypertension:https://pubmed.ncbi.nlm.nih.gov/16232127/
- Is there a role for 5-HT1A agonists in the treatment of depression?:https://pubmed.ncbi.nlm.nih.gov/12559651/
- 5-HT1A receptor antagonists reduce food intake and body weight by reducing total meals with no conditioned taste aversion:https://pubmed.ncbi.nlm.nih.gov/24064183/
- The role of serotonin and its receptors in activation of immune responses and inflammation:https://pubmed.ncbi.nlm.nih.gov/25439045/
- The influence of ketamine on drug discovery in depression:https://pubmed.ncbi.nlm.nih.gov/31382015/
- Antidepressant-like effects of ecstasy in subjects with a predisposition to depression:https://pubmed.ncbi.nlm.nih.gov/22704044/
- Antidepressant-like effects of 3,4-methylenedioxymethamphetamine in an animal model of depression:https://pubmed.ncbi.nlm.nih.gov/21979832/
- The medical benefit of 5-HT research:https://pubmed.ncbi.nlm.nih.gov/11888547/
- Methylone, a rapid acting entactogen with robust anxiolytic and antidepressant-like activity:https://pubmed.ncbi.nlm.nih.gov/36704743/
- The promise of ketamine for treatment-resistant depression: current evidence and future directions:https://pubmed.ncbi.nlm.nih.gov/25649308/
- Here Are 4 Conditions That the Drug Ecstasy May Help Treat:https://www.healthline.com/health-news/4-conditions-that-ecstasy-may-help-treat
- Psilocybin’s Potential Mechanisms in the Treatment of Depression: A Systematic Review:https://pubmed.ncbi.nlm.nih.gov/37385217/
- Magic Mushroom Compound Called Psilocybin May Help Treat Depression:https://www.healthline.com/health-news/magic-mushroom-compound-called-psilocybin-may-help-treat-depression
- Harnessing psilocybin: antidepressant-like behavioral and synaptic actions of psilocybin are independent of 5-HT2R activation in mice:https://pubmed.ncbi.nlm.nih.gov/33850049/
- Could Magic Mushrooms Ever Replace Today’s Antidepressants?:https://www.healthline.com/health-news/could-magic-mushrooms-ever-replace-ssris
- What Is Ayahuasca? Experience, Benefits, and Side Effects:https://www.healthline.com/nutrition/ayahuasca
- Ayahuasca for the Treatment of Depression:https://pubmed.ncbi.nlm.nih.gov/34761362/
- Rapid antidepressant effects of the psychedelic ayahuasca in treatment-resistant depression: a randomized placebo-controlled trial:https://pubmed.ncbi.nlm.nih.gov/29903051/
- Ayahuasca’s Antidepressant Effects Covary with Behavioral Activation as Well as Mindfulness:https://pubmed.ncbi.nlm.nih.gov/31570056/
- Ayahuasca, a potentially rapid acting antidepressant: focus on safety and tolerability:https://pubmed.ncbi.nlm.nih.gov/35301934/
- Banisteriopsis caapi, a unique combination of MAO inhibitory and antioxidative constituents for the activities relevant to neurodegenerative disorders and Parkinson’s disease:https://pubmed.ncbi.nlm.nih.gov/19879939/
- Composition, standardization and chemical profiling of Banisteriopsis caapi, a plant for the treatment of neurodegenerative disorders relevant to Parkinson’s disease:https://pubmed.ncbi.nlm.nih.gov/20219660/
- The alkaloids of Banisteriopsis caapi, the plant source of the Amazonian hallucinogen Ayahuasca, stimulate adult neurogenesis in vitro:https://pubmed.ncbi.nlm.nih.gov/28706205/
- Psychotria viridis: Chemical constituents from leaves and biological properties:https://pubmed.ncbi.nlm.nih.gov/28640347/
- IDENTIFICATION CHALLENGES IN EXAMINATION OF COMMERCIAL PLANT MATERIAL OF PSYCHOTRIA VIRIDIS:https://pubmed.ncbi.nlm.nih.gov/26647632/
- Ayahuasca: Psychological and Physiologic Effects, Pharmacology and Potential Uses in Addiction and Mental Illness:https://pubmed.ncbi.nlm.nih.gov/29366418/
- Ayahuasca: What Healthcare Providers Need to Know:https://pubmed.ncbi.nlm.nih.gov/34060770/
- Biochemistry, Serotonin:https://pubmed.ncbi.nlm.nih.gov/32809691/
- Neuropharmacology of N,N-dimethyltryptamine:https://pubmed.ncbi.nlm.nih.gov/27126737/
- Is mindfulness Buddhist? (and why it matters):https://pubmed.ncbi.nlm.nih.gov/25361692/
- What defines mindfulness-based programs? The warp and the weft:https://pubmed.ncbi.nlm.nih.gov/28031068/
- Mindfulness in healthcare professionals and medical education:https://pubmed.ncbi.nlm.nih.gov/33223537/
- Mindfulness, Multitasking, and You:https://pubmed.ncbi.nlm.nih.gov/26844712/
- Moving Mindfully: The Role of Mindfulness Practice in Physical Activity and Health Behaviours:https://pubmed.ncbi.nlm.nih.gov/33578852/
- The benefits of meditation and mindfulness practices during times of crisis such as COVID-19:https://pubmed.ncbi.nlm.nih.gov/32406348/
- The pharmacology of sigma-1 receptors:https://pubmed.ncbi.nlm.nih.gov/19619582/
- The Sigma-1 receptor is an ER-localized type II membrane protein:https://pubmed.ncbi.nlm.nih.gov/34648767/
- How Dextromethorphan Is Used for the Treatment of Depression:https://www.healthline.com/health/depression/dextromethorphan-for-depression
- Everything You Need to Know About Robotripping:https://www.healthline.com/health/robotripping
- Psilocybin-assisted therapy for depression: How do we advance the field?:https://pubmed.ncbi.nlm.nih.gov/31752499/
- Single Dose of Synthetic ‘Magic Mushroom’ Psilocybin Eases Severe Depression:https://www.healthline.com/health-news/single-dose-of-synthetic-magic-mushroom-psilocybin-eases-severe-depression
- Harnessing psilocybin: antidepressant-like behavioral and synaptic actions of psilocybin are independent of 5-HT2R activation in mice:https://pubmed.ncbi.nlm.nih.gov/33850049/
- FDA Puts ‘Magic Mushroom’ Ingredient on Fast Track for Depression Treatment:https://www.healthline.com/health-news/fda-looking-at-magic-mushroom-ingredient-to-treat-depression
- Sevoflurane. A review of its pharmacodynamic and pharmacokinetic properties and its clinical use in general anaesthesia:https://pubmed.ncbi.nlm.nih.gov/8706599/
- Sevoflurane in paediatric anaesthesia: a review:https://pubmed.ncbi.nlm.nih.gov/10937447/
- Sevoflurane: are there differences in products?:https://pubmed.ncbi.nlm.nih.gov/17513639/
- Sevoflurane augmentation in treatment-resistant depression: a clinical case study:https://pubmed.ncbi.nlm.nih.gov/35186257/
- Inhaled anesthetic agents:https://pubmed.ncbi.nlm.nih.gov/16554286/
- The effects of the general anesthetic sevoflurane on neurotransmission: an experimental and computational study:https://pubmed.ncbi.nlm.nih.gov/33619298/
- Mechanisms of the beneficial effect of sevoflurane in liver ischemia/reperfusion injury:https://pubmed.ncbi.nlm.nih.gov/26647794/
- Electrophysiologic mechanism underlying action potential prolongation by sevoflurane in rat ventricular myocytes:https://pubmed.ncbi.nlm.nih.gov/17585217/
- The action of sevoflurane on vascular smooth muscle of isolated mesenteric resistance arteries (part 2): mechanisms of endothelium-independent vasorelaxation:https://pubmed.ncbi.nlm.nih.gov/10781291/
- Emerging evidence for antidepressant actions of anesthetic agents:https://pubmed.ncbi.nlm.nih.gov/29794854/
- Antidepressants 101: Pros and Cons:https://www.healthline.com/health/depression/antidepressants-pros-and-cons
- What Medications Help Treat Depression?:https://www.healthline.com/health/depression/medication-list
- The role of calcium in the energetics of contracting skeletal muscle:https://pubmed.ncbi.nlm.nih.gov/1664541/
- Calcium ion in skeletal muscle: its crucial role for muscle function, plasticity, and disease:https://pubmed.ncbi.nlm.nih.gov/10893434/
- Antidepressant effects of the muscarinic cholinergic receptor antagonist scopolamine: a review:https://pubmed.ncbi.nlm.nih.gov/23200525/
- The antidepressant efficacy of the muscarinic antagonist scopolamine: Past findings and future directions:https://pubmed.ncbi.nlm.nih.gov/32616213/
- Scopolamine as an antidepressant: a systematic review:https://pubmed.ncbi.nlm.nih.gov/23334071/
- GABA interneurons mediate the rapid antidepressant-like effects of scopolamine:https://pubmed.ncbi.nlm.nih.gov/27270172/
- Mitochondrial involvement in memory impairment induced by scopolamine in rats:https://pubmed.ncbi.nlm.nih.gov/28398193/
- Antidepressants 101: Pros and Cons:https://www.healthline.com/health/depression/antidepressants-pros-and-cons
- Rapid-Acting Antidepressants:https://pubmed.ncbi.nlm.nih.gov/30058481/
- Discovery of subtype selective muscarinic receptor antagonists as alternatives to atropine using in silico pharmacophore modeling and virtual screening methods:https://pubmed.ncbi.nlm.nih.gov/23523385/
- Muscarinic receptor subtypes and management of the overactive bladder:https://pubmed.ncbi.nlm.nih.gov/12493364/
- Physiology, Cholinergic Receptors:https://pubmed.ncbi.nlm.nih.gov/30252390/
- The Diagnosis and Treatment of Unipolar Depression:https://pubmed.ncbi.nlm.nih.gov/37070271/
- Bipolar disorder:https://pubmed.ncbi.nlm.nih.gov/26388529/
- Everything You Need to Know About Bipolar Disorder:https://www.healthline.com/health/bipolar-disorder
- Bipolar disorders:https://pubmed.ncbi.nlm.nih.gov/29516993/